
Unidade 1 Estudo da matéria

Os materiais e a construção civil
A escolha adequada do material a ser utilizado em uma construção, seja para fins estéticos, seja para fins funcionais, está relacionada com as propriedades químicas e físicas dêsse material.
Respostas e comentários
Objetivos da Unidade
• Compreender as diferenças e as similaridades entre Química e Física.
• Descrever algumas aplicações cotidianas tanto de Física quanto de Química.
• Definir matéria.
• Observar fenômenos naturais interpretando suas características físicas e químicas.
• Compreender as mudanças de estado físico no nível submicroscópico e macroscópico.
• Comparar experimentalmente materiais no que diz respeito a mudanças de estado físico.
• Ampliar o conhecimento sôbre as diferenças de estado físico da matéria por meio de modelos de partículas.
• Diferenciar as propriedades gerais e específicas da matéria.
• Reconhecer a massa e o volume como propriedades gerais da matéria e a densidade como uma propriedade específica da matéria.
• Conhecer as unidades de medida padrão no ésse Í para massa, volume e densidade.
• Verificar algumas propriedades específicas da matéria com relação ao seu estado físico.
• Comparar materiais de mesma massa ou de mesmo volume e diferentes densidades.
• Associar diferentes propriedades da matéria aos estados físicos.
• Compreender os efeitos da temperatura e da pressão sôbre as propriedades e os estados físicos da matéria.
• Reconhecer a contribuição de Rosalind Franklin e outras mulheres para a Ciência e as dificuldades por elas enfrentadas.
• Refletir sôbre o descarte de medicamentos e os possíveis impactos ambientais e na saúde humana decorrentes do descarte inadequado.
• Analisar dados sôbre a variação de temperatura global e mudanças no nível médio dos oceanos decorrentes do aquecimento global.
• Organizar dados coletados em entrevistas.
• Comparar experimentalmente mudanças de estado físico de diferentes materiais.
• Analisar curvas de aquecimento e de resfriamento.
• Construir um aparato para avaliar a densidade de líquidos.
• Contribuir para a conservação do ambiente com atitudes sustentáveis.
Temas contemporâneos transversais (tê cê tês) em foco nesta Unidade
• Educação em Direitos Humanos: promover reflexões sôbre a importância do respeito à diversidade nos diversos setores da sociedade.
• Educação Ambiental: refletir sôbre os impactos das ações humanas e a necessidade do descarte adequado de medicamentos e de outros materiais para a conservação do ambiente.
Habilidades da Bê êne cê cê em foco nesta Unidade
• ê éfe zero nove cê ih zero um: Investigar as mudanças de estado físico da matéria e explicar essas transformações com base no modêlo de constituição submicroscópica.
• ê éfe zero nove cê ih um três: Propor iniciativas individuais e coletivas para a solução de problemas ambientais da cidade ou da comunidade, com base na análise de ações de consumo consciente e de sustentabilidade bem-sucedidas.
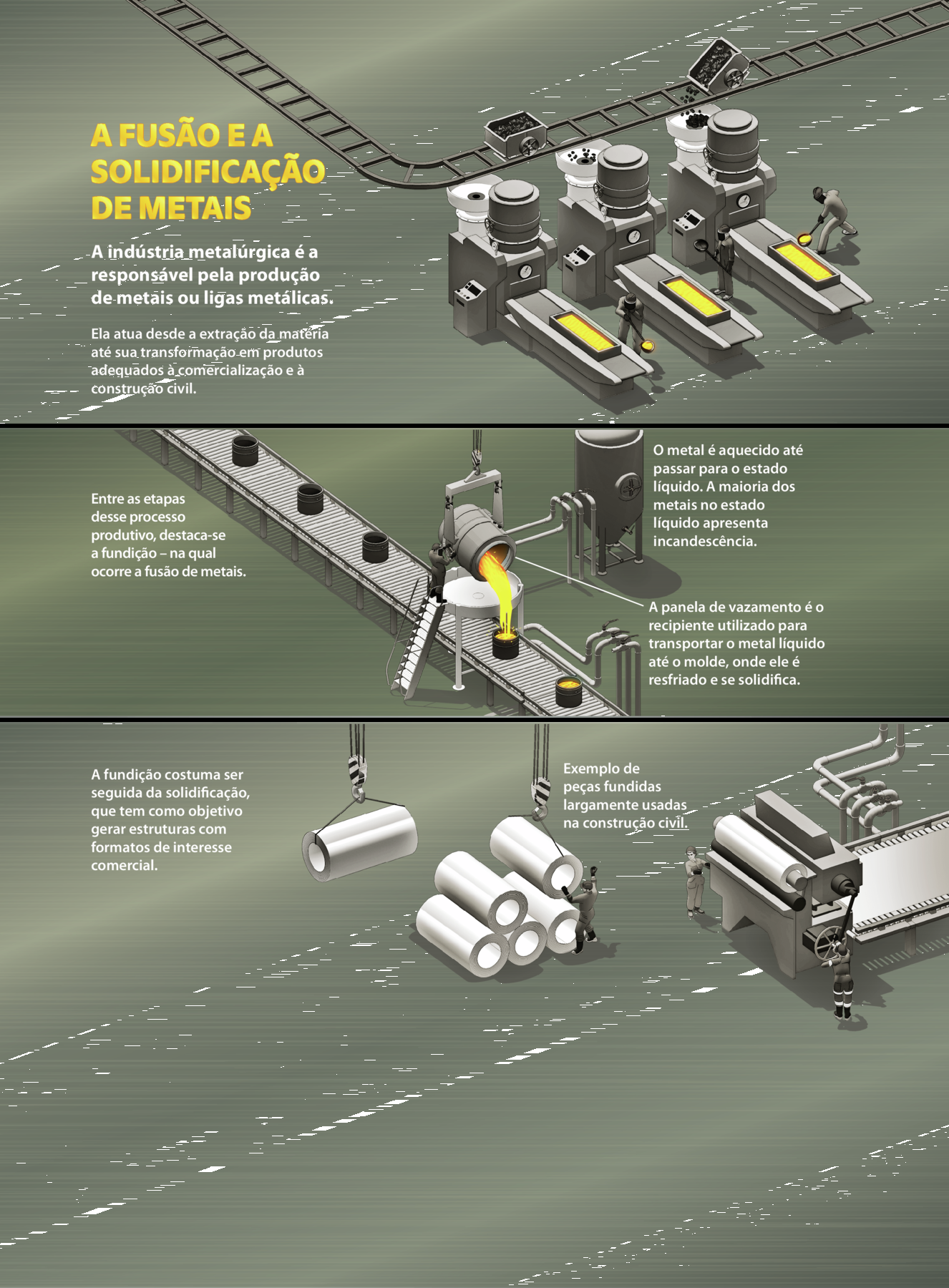
Começando a Unidade
- Cite exemplos de materiais conhecidos que se encontram nos estados sólido, líquido ou gasoso.
- Quais mudanças de estado físico ocorrem com os metais nos processos de fundição e moldagem empregados na indústria metalúrgica?
- Por que pedaços de metais afundam quando inseridos em um recipiente com água?
Por que estudar esta Unidade?
Compreender as diferentes propriedades da matéria dependendo de seu estado físico e como ocorrem as mudanças de estado. Por meio dessa compreensão é possível explicar quais são as diferenças entre a água líquida presente nos oceanos e o vapor de água encontrado na atmosfera.
A observação de fenômenos da natureza e a busca por essas e outras respostas auxiliaram o ser humano no desenvolvimento de processos industriais que possibilitaram a criação de produtos com base na mudança de estado físico dos materiais.
Respostas e comentários
Orientações didáticas
• Antes de iniciar esta Unidade, questione os estudantes sôbre os estados físicos da água, os quais foram trabalhados em anos anteriores. Resgatar alguns conhecimentos prévios, sobretudo aqueles relacionados às mudanças de estado físico, permitirá aos estudantes gerar inferências durante a leitura desta Unidade.
• Ao analisar as imagens de abertura, faça perguntas como: “Qual é o estado físico da maioria dos metais?”; “O que é necessário fazer para que um metal apresente fórmas diferentes, como na estrutura do teatro da foto?”.
• Comente com os estudantes que as propriedades da matéria ajudam a explicar a aplicação de alguns materiais extraídos da natureza ou obtidos artificialmente. Promova uma discussão sôbre as diferentes aplicações de materiais distintos, como a madeira e os plásticos, relacionando-os às suas propriedades.
Respostas – Começando a Unidade
1. Resposta pessoal. Os estudantes podem mencionar diferentes tipos de material, como objetos sólidos, bebidas e vapor de água.
2. Na fundição, os sólidos se tornam líquidos, enquanto na moldagem os líquidos se transformam em sólidos.
3. Os metais têm densidade maior que a da água. É possível que os estudantes respondam que o metal afunda porque é mais pesado. Retome essas respostas ao trabalhar o tópico sôbre densidade.

TEMA 1 Áreas da Ciência que investigam a matéria
A Química e a Física são Ciências que procuram explicar a matéria, suas interações e suas transformações.
Você sabe do que é feita a água? Por que ela pode ser encontrada na natureza nos estados sólido, líquido e gasoso? Como podemos tornar potável a água de rios e lagos?
Essas perguntas têm respostas porque muitos estudos foram realizados com o objetivo de entender os fenômenos que ocorrem na natureza. Com base em seus objetos de estudo e nos métodos utilizados, as pessoas que investigam os fenômenos naturais foram, ao longo do tempo, especializando-se em diferentes áreas da Ciência, como a Química e a Física.
Com o avanço científico e tecnológico e a integração de diferentes áreas do conhecimento, é possível propor aplicações práticas para questões da atualidade, como a cura de doenças ou a redução da poluição ambiental.
A Química
A Química investiga a estrutura, a composição, as propriedades e as transformações da matéria. Nesse sentido, considera-se matéria tudo o que tem massa e ocupa lugar no espaço.
A curiosidade sôbre a constituição da matéria é antiga; registros históricos mostram que a primeira tentativa de entender os fenômenos naturais e explicar a constituição da matéria de fórma desvinculada da religião ocorreu há cêrca de 2.500 anos, na Grécia. Posteriormente, a partir do século dezenove, experimentos foram capazes de evidenciar que a matéria era constituída de partículas invisíveis a ôlho nu.
Atualmente, a definição de matéria engloba estruturas que não conseguimos ver a ôlho nu. Os cristais de cloreto de sódio (principal constituinte do sal de cozinha) destacados na imagem, por exemplo, têm massa e volume e, portanto, são considerados matéria.

A Física
Na Física, os cientistas também se dedicam a compreender as propriedades da matéria, mas o foco não está em suas transformações, e sim em como ela interage com a própria matéria e com certos fenômenos – como luz, calor e eletricidade –, no decorrer do tempo e no espaço. Ao longo do tempo, foram desenvolvidos equipamentos e métodos que auxiliam os físicos na compreensão dêsses aspectos.
Respostas e comentários
Orientações didáticas
• Ao longo desta Unidade, trabalhe continuamente a observação crítica e a interpretação dos fenômenos que forem apresentados, tais como os relativos ao volume, à densidade e ao estado físico da matéria, favorecendo o desenvolvimento da competência específica 3 de Ciências da Natureza para o Ensino Fundamental, prevista pela Bê êne cê cê.
• Ao apresentar a Química e a Física como ramos diferentes das Ciências da Natureza, garanta que os estudantes percebam que ambas as Ciências estudam a matéria, porém com perspectivas distintas. Enquanto a Física busca explicações energéticas e constitutivas, bem como as forças universais exercidas sôbre a matéria, a Química estuda a estrutura, a composição, as propriedades e a reatividade da matéria. Essas Ciências são interdependentes e seus estudos se complementam.
• Destaque que, além dos experimentos, os cientistas também fazem o tratamento dos dados experimentais, a discussão dos resultados e o planejamento das etapas seguintes para que a equipe de pesquisa atinja os objetivos propostos no experimento. Caso perceba que os estudantes assumam que a Ciência é estática e acabada, ressalte que ela apresenta uma construção humana coletiva ao longo do tempo e que a colaboração entre diferentes áreas do conhecimento é muito importante. Assim, é possível trabalhar parcialmente a competência geral 1 da Educação Básica e as competências específicas 1 e 2 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê.
Saiba mais!
A IMPORTÂNCIA DOS EVENTOS CIENTÍFICOS
A primeira conferência internacional de Física foi realizada em 1911, no Instituto Internacional da de Física e Química, localizado na Bélgica e fundado pelo químico (1838-1922). As Conferências de são importantes congressos internacionais que, ao reunir físicos e químicos, permitem a discussão de resultados experimentais e teorias, impulsionando o desenvolvimento da Ciência.
Muitos outros eventos científicos são realizados ao redor do planeta. Alguns são organizados em torno de temas muito específicos, como no caso das Conferências de . Outros, envolvem tópicos de muitas áreas do conhecimento, como as reuniões anuais da Sociedade Brasileira para o Progresso da Ciência. Esses eventos têm grande importância no processo da comunicação científica, pois novas ideias e novos dados experimentais chegam ao conhecimento dos participantes de maneira mais rápida e interativa. Além disso, eles possibilitam a concretização de parcerias entre instituições de pesquisa e ensino de diferentes países.

De ôlho no tema
Para aquecer a água, podemos utilizar a chama do fogão, que é produzida pela combustão do gás de cozinha. Esse processo envolve a transferência de energia na fórma de calor.
O aquecimento da água a partir da transformação do gás em chama pode ser objeto de estudo da Física? E da Química? Explique sua resposta.
Respostas e comentários
Orientações didáticas
• Ao trabalhar o quadro Saiba mais!, destaque a importância da troca de informações entre pesquisadores e dos congressos e outros eventos científicos para a divulgação de pesquisas realizadas em indústrias e universidades. As Ciências são complementares, e o trabalho em conjunto dos cientistas auxilia na contínua evolução das pesquisas científicas. O compartilhamento de resultados entre estudiosos do mundo inteiro em congressos também possibilita essa progressão.
• Ao discutir a questão, mencione Marie Curie como a única mulher cientista na foto. Instigue-os a refletir sôbre as possíveis razões para esse fato. Você pode mencionar a história de Malala iuçáfizái (1997-), uma estudante paquistanesa ganhadora do prêmio Nobel da paz em 2014 por sua luta pelo direito especialmente das meninas ao acesso à educação. Essa proposta oportuniza o trabalho com o tê cê tê– Educação em Direitos Humanos.
Resposta – De ôlho no tema
Esse processo pode ser objeto de estudo tanto da Física quanto da Química, pois envolve a transformação da matéria (produção da chama) e a transferência de energia na fórma de calor. Se julgar conveniente, esclareça que a Química e a Física são campos tão interdisciplinares que existe um campo específico chamado Físico-Química, que estuda as propriedades da matéria pela combinação das duas Ciências. Além disso, evidencie que, embora exista a compartimentalização do conhecimento em Química e Física, o trabalho dos cientistas não apresenta fronteiras tão rígidas. É natural o trabalho de pesquisa buscar conhecimentos de outras áreas.
Sugestão de recurso complementar
Artigo
10 grandes mulheres da Ciência. Galileu, 8 março. 2017.
O texto apresenta a área de atuação de 10 grandes cientistas mulheres e a época em que viveram.
Disponível em: https://oeds.link/KrPQmd. Acesso em: 11 agostoponto 2022.

TEMA 2 Propriedades gerais e específicas da matéria
A matéria apresenta propriedades gerais e específicas.
Agora sabemos que matéria é tudo aquilo que tem massa e ocupa lugar no espaço. Os livros, os lápis, o ar, a água e nosso corpo são exemplos de matéria. Uma porção limitada de matéria pode ser chamada de corpo. Um corpo produzido pelo ser humano para uma finalidade específica é denominado objeto.
Propriedades gerais da matéria são aquelas comuns a todo tipo de corpo. A massa, o volume e a impenetrabilidade são exemplos, pois são comuns a todos os corpos, independentemente de sua composição.
Propriedades específicas da matéria são aquelas que dependem do material de que é composto um corpo. A densidade é um exemplo de propriedade específica.
Massa
A massa é a propriedade relacionada com a quantidade de matéria que um corpo possui. A massa dos corpos é medida diretamente por meio de instrumentos chamados balanças. A unidade padrão de medida de massa no Sistema Internacional de Unidades ésse í é o quilograma (quilograma).
Volume e impenetrabilidade
O volume de um corpo é a medida do espaço que ele ocupa, o que pode ser determinado pelas suas dimensões. Por exemplo, o volume de um sólido geométrico, como o cubo ou o paralelepípedo, é obtido pela multiplicação das medidas da altura, da largura e da profundidade dele.
Volume de um cubo
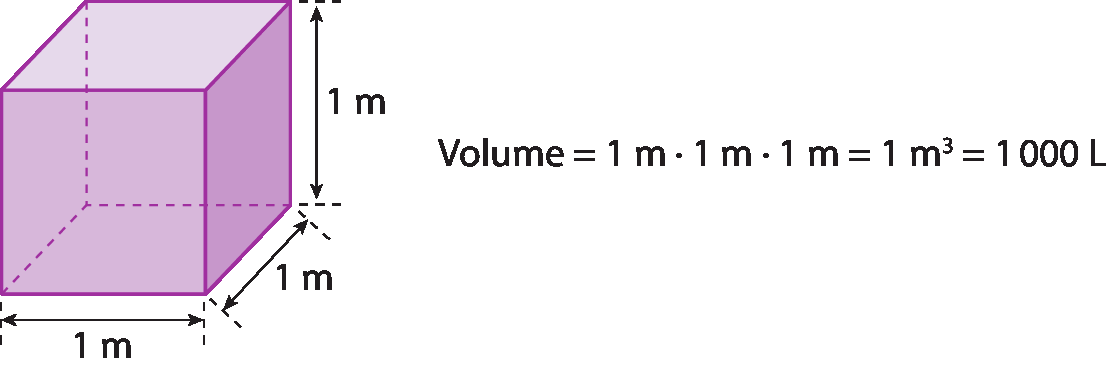
Para medição de volume de líquidos é comum o uso de instrumentos de medida com graduações, como as provetas.
Respostas e comentários
Orientações didáticas
• Garanta que os estudantes entendam a diferença entre matéria, corpo e objeto. Esclareça que matéria é tudo o que possui massa e volume no espaço; corpo, na Física e na Química, corresponde a uma porção parcial, limitada da matéria; já os objetos são corpos aos quais o ser humano atribui uma utilidade. Todo objeto é também um corpo e uma matéria, assim como todo corpo é também uma matéria. Pode-se exemplificar com diferentes terminologias para o ouro: minério de ouro (matéria), ouro metálico extraído (corpo), anel de ouro (objeto).
• Reforce que massa e volume são propriedades gerais e independem de quais são os constituintes da matéria.
• Nessa etapa, os estudantes ainda podem ter dificuldade de distinguir corretamente os conceitos de massa e pêso. Retome os conhecimentos prévios, lembrando-os de que, quando subimos em uma balança, estamos medindo a massa que compõe nosso corpo. Essa medida é determinada pela balança, que quantifica a massa de um corpo. Comente que, apesar de a maioria das pessoas relacionar o valor obtido na balança ao seu peso, em Ciências o uso dêsse termo não é correto, uma vez que o pêso é uma grandeza que relaciona a massa e a aceleração da gravidade. Ressalte que a distinção entre massa e pêso pode ser identificada na indicação da unidade de medida, que para a massa, no Sistema Internacional de Unidades (ésse Í), é quilograma e para o pêso é quilograma · métro por segundo ao quadrado.
No ésse Í, a unidade de medida de comprimento é o metro; para o volume, a unidade de medida é o metro cúbico (m³). É comum utilizarmos, no dia a dia, as unidades litro (L) e mililitro (mL) para nos referirmos ao volume de um corpo. O volume de 1 metro cúbico corresponde a 1 000 litros ou 1 000 000 mililitros.
O volume de um corpo depende da temperatura e da pressão em que ele se encontra. Você vai entender melhor essa relação ao estudar o Tema 3 desta Unidade.
Como cada corpo ocupa lugar no espaço, dois corpos não podem ocupar o mesmo lugar no espaço ao mesmo tempo. Essa propriedade é chamada de impenetrabilidade e está representada na imagem a seguir. Ao colocar uma pedra em um recipiente completamente cheio de água, o líquido vai transbordar, pois o sólido passou a ocupar parte do espaço da água.
Impenetrabilidade

Saiba mais!
SISTEMA INTERNACIONAL DE UNIDADES (SI)
O ésse Í é adotado em diversos países para padronizar unidades de medidas e assim facilitar a comunicação, principalmente no meio científico e nas transações comerciais. As unidades básicas do ésse Í são: o metro (m), para comprimento; o segundo (s), para tempo; o quilograma (kg), para massa; o ampere (A), para corrente elétrica; o kelvin (K), para temperatura; o mol (mol), para quantidade de matéria; e o candela (cd), para intensidade luminosa. Com as unidades do ésse Í, é possível expressar todas as grandezas físicas conhecidas.
Densidade
As propriedades gerais da matéria não podem ser empregadas para diferenciar um material de outro. Já um conjunto de propriedades específicas, como a densidade, pode ser utilizado com essa finalidade.
Densidade é a razão entre a massa e o volume de um corpo, em determinadas condições de temperatura e pressão.
Matematicamente, a densidade de um corpo (d ) é o resultado da divisão de sua massa (m) por seu volume (V ).
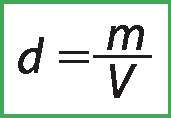
Respostas e comentários
Orientações didáticas
• Explique aos estudantes que eles devem associar o termo volume ao espaço ocupado por um corpo. Para algumas figuras geométricas, o volume pode ser calculado com base nas medidas do comprimento de suas arestas, como é o caso do cubo. Se julgar conveniente, aborde colaborativamente com o professor do componente curricular Matemática o estudo do cálculo do volume de sólidos geométricos, como o cilindro e o paralelepípedo, favorecendo a assimilação dessas equações e o significado da unidade metro cúbico. Atente-se à diferença entre volume e capacidade. O volume corresponde à medida do espaço que o corpo ocupa, e a capacidade corresponde à quantidade de espaço que o fluido ocupa no interior de um recipiente.
• Para objetos com formato complexo, pode ser usado o método indireto, que permite medir seu volume considerando a propriedade geral da impenetrabilidade – dois corpos não podem ocupar o mesmo lugar no espaço. Uma opção de abordagem para trabalhar o conceito de impenetrabilidade é apresentar aos estudantes o problema da determinação do volume de sólidos irregulares e pedir a eles que proponham métodos experimentais para realizar a medida, como preencher completamente com água um recipiente com dimensões conhecidas, inserir o objeto com fórma complexa nele e medir o volume de água que transborda. Discuta com eles os métodos propostos, sugerindo somente alterações que eliminem riscos, permitindo que eles aprendam com seus eventuais erros durante a atividade prática e aperfeiçoem seus métodos, favorecendo o trabalho com a competência geral 2 da Educação Básica e as competências específicas 2 e 3 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê.
• Aproveite e relacione as propriedades da matéria com sua constituição atômica. Algumas propriedades dependem dos átomos que compõem a matéria. Por exemplo, materiais compostos de átomos de elementos químicos de maior número atômico possuem maior massa; portanto, a densidade (massa em função do volume ocupado) depende diretamente de quais são seus átomos constituintes.
Sugestão de recurso complementar
Artigo
CESAR, J.; DE PAOLI, M. A.; ANDRADE, J. C. A determinação da densidade de sólidos e líquidos. Chemkeys, Campinas: Editora da unicâmpi, número 7, 2004.
O artigo propõe uma abordagem mais ampla do conceito de densidade e apresenta alguns procedimentos de laboratório para a determinação da densidade de materiais.
Disponível em: https://oeds.link/Kmwn7f. Acesso em: 11 agosto 2022.
No ésse Í, a densidade deve ser expressa em quilograma por metro cúbico (cá gê barra ême elevado a três). É comum, porém, expressarmos a densidade em gramas por centímetro cúbico (gê barra cê ême elevado a três). A relação entre essas unidades é: 1 = 0,001 grama por centímetro cúbico.
Para esclarecer a relação entre massa e volume na determinação da densidade, vamos recorrer a um exemplo: comparar cubos de mesmas dimensões, mas de materiais diferentes.
Nas mesmas condições de temperatura e pressão, ao comparar um cubo de madeira com um cubo de ferro de mesmo volume, verificamos que eles apresentam densidades diferentes, pois têm massas distintas.
Na figura a seguir, estão representados cubos de madeira e de ferro com o mesmo volume de 1.000 centímetros. O desnível da balança deve-se aos diferentes valores de massa: o corpo de ferro tem massa maior que a do corpo de madeira.
Comparação de materiais com densidades diferentes
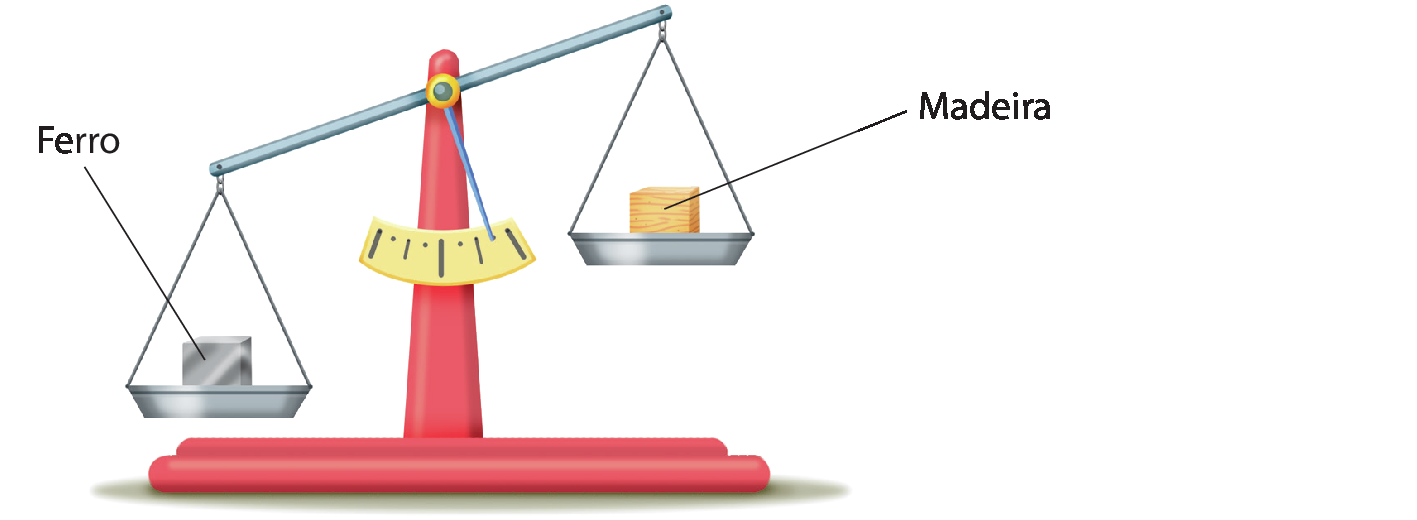
Como os cubos têm o mesmo volume, mas o cubo de ferro tem massa maior, podemos concluir, então, que a densidade do cubo de ferro é maior que a do cubo de madeira.
O mesmo raciocínio pode ser aplicado comparando corpos distintos de mesma massa. Vamos analisar o caso do açúcar refinado e do sal de cozinha. Nas mesmas condições de temperatura e pressão, esses corpos ocupam volumes diferentes; 1 quilograma de açúcar comum ocupa um volume maior que 1 quilograma de sal de cozinha. Portanto, é possível concluir que os corpos possuem densidades diferentes e que o sal de cozinha é mais denso que o açúcar comum.

Respostas e comentários
Orientações didáticas
• Ao abordar as unidades de medida de massa, volume e densidade, segundo o ésse Í, estabeleça a relação entre a unidade e os parâmetros utilizados para definir cada propriedade. Por exemplo, a densidade é definida considerando-se o volume (métro cúbico) e a massa (quilograma) do objeto; assim, a unidade que a representa é .
• Pelo senso comum, é frequente o emprêgo dos adjetivos “leve” e “pesado” como sinônimos de pouco e muito denso, respectivamente. Isto é, associa-se a densidade apenas à massa dos materiais. Pode-se estimular a reflexão dos estudantes sôbre a necessidade de considerar também o volume por meio de algumas questões que evidenciem sua importância, tal como: “Se colocarmos em uma balança um recipiente contendo 1 litro de água, retirá-lo e colocarmos em seguida outro recipiente idêntico, mas contendo 1 litro de óleo de cozinha, as massas medidas serão iguais?”; “Por que isso acontece?”. Ou, ainda: “Um cubo de 1 quilograma de chumbo ocupa o mesmo espaço que um cubo de 1 quilograma de algodão?”.
• Considere levar para a sala de aula objetos com mesmo volume e massas distintas e uma balança. Dessa fórma, concretiza-se o que foi representado na imagem “Comparação de materiais com densidades diferentes”, auxiliando na compreensão do conceito de densidade. Também é interessante comparar os volumes de 100 gramas de algodão e 100 gramas de ferro, por exemplo.
• Após o estudo do conceito de densidade, a seção Explore – Construindo um instrumento para análise da densidade de líquidos pode ser trabalhada, já que tem como objetivo verificar a densidade de diferentes materiais, comparando-os pelo uso de um densímetro construído pelos próprios estudantes.
A densidade de um corpo pode ser alterada pela adição de outro material. Por exemplo, a densidade de um balão de borracha vazio é diferente da densidade do mesmo balão cheio de ar.
As mudanças de estado físico também podem alterar a densidade de um material. Por exemplo, a água líquida tem densidade 1 grama por centímetro cúbico, e a água sólida (gêlo) tem densidade 0,92 grama por centímetro cúbico. A densidade de um material também pode variar em razão da temperatura e da pressão em que se encontra. Por exemplo, ao nível do mar e a 25 graus Célsius, a água apresenta densidade 1,00 grama por centímetro cúbico, e a 100 graus Célsius a densidade da água é 0,95 grama por centímetro cúbico. Por isso, as condições de pressão e de temperatura são geralmente registradas nas tabelas de densidade, como está representado a seguir.
Verifique e compare os valores da densidade dos materiais fornecidos na tabela. Note que cada material apresenta um valor de densidade; por isso, a densidade é considerada uma propriedade específica da matéria e pode ser empregada para diferenciar um material de outro.
|
Material |
Densidade (g/cm3) |
|---|---|
|
Mercúrio |
13,50 |
|
Chumbo |
11,30 |
|
Alumínio |
2,70 |
|
Quartzo |
2,65 |
|
Cloreto de sódio |
2,17 |
|
Água |
1,00 |
|
Sódio |
0,97 |
Fonte: LIDE, R. D. editor. cê érre cê Handbook of Chemistry and Physics. 90. edição (cedê-Versão 2010). Boca Raton: CRC Press/Taylor and Francis, 2009.
Saiba mais!
DENSIDADE E FLUTUAÇÃO
Um fenômeno que envolve a densidade dos materiais é a flutuação. Quando um corpo é colocado em um líquido, ele afunda se tiver densidade maior que a dêsse líquido e flutua se sua densidade for menor.
Entrando na rede
Na página do PhET Interactive Simulations, disponível em: https://oeds.link/x50i8vnsity/latest/density_pt_BR.html, há um simulador para que você possa comparar a densidade de diferentes materiais.
Acesso em: 7 agosto 2022.
De ôlho no tema
Garrafas de plástico lançadas ao mar costumam flutuar. Entretanto, quando cheias de água, elas afundam.
- Qual propriedade explica o fenômeno descrito?
- Qual outra propriedade se altera após se adicionar água na garrafa?
- Como as duas propriedades dos itens anteriores estão relacionadas?
- Se a garrafa fosse preenchida com outro material, como o mercúrio ou o sódio, ainda afundaria?
Respostas e comentários
Orientações didáticas
• Ao trabalhar a tabela “Densidade de alguns materiais”, espera-se que os estudantes percebam que materiais como mercúrio e alumínio são mais facilmente diferenciados com base em suas densidades, já que apresentam valores bastante distintos dessa propriedade. Pode-se também notar que, para distinguir alumínio de quartzo, ou água de sódio, essa propriedade não é a mais indicada. Nesses casos, os materiais podem ser diferenciados por meio de outras características, como côr e brilho.
• Caso julgue oportuno, organize a turma em grupos e peça que providenciem bacias com água. Oriente os estudantes a escolher objetos do dia a dia, indicando, antes da execução da atividade, quais objetos afundarão ao serem colocados na água. Peça que façam o teste e analisem os resultados, elaborem explicações e verifiquem se eles corroboram a hipótese inicial. Além disso, solicite a eles que classifiquem a densidade dos objetos testados em relação à densidade da água, com base nos resultados.
• Ao trabalhar as questões do quadro De ôlho no tema, pode-se discutir com os estudantes a poluição gerada pelos plásticos descartados inadequadamente nos oceanos para entender o impacto dessa ação, favorecendo o trabalho com o tê cê tê – Educação Ambiental.
Respostas – De ôlho no tema
a) Densidade.
b) A garrafa cheia de água apresenta maior massa que a vazia, por isso sua densidade aumenta. O conjunto garrafa e água apresenta uma densidade maior que a água, por isso ele afunda.
c) A densidade é a razão entre a massa e o volume de um corpo, em condições específicas de temperatura e de pressão.
d) A garrafa preenchida com mercúrio afundaria, por ter maior densidade que a água do mar, e a garrafa preenchida com sódio flutuaria, por ter menor densidade que a água do mar.
Sugestão de recurso complementar
Artigo
párquer, L. Em 2040, lixo plástico nos oceanos poderá ser o triplo do atual. National Geographic Brasil, 5 novembro 2020.
O texto aborda o impacto dos resíduos de plásticos nos oceanos.
Disponível em: https://oeds.link/rbMXDV. Acesso em: 11 agosto 2022.

Atividades
TEMAS 1 E 2
REGISTRE EM SEU CADERNO
ORGANIZAR
1. Considere o paralelepípedo representado pela figura e responda às questões.
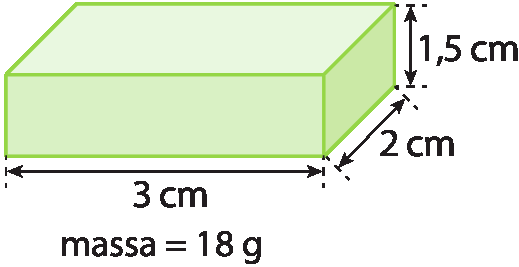
- Qual é o seu volume?
- Qual é a sua densidade em quilogramas por métro cúbico?
ANALISAR
2. Um bom argumento é aquele em que premissas são verdadeiras e apoiam a conclusão. Já em um discurso falso, ou seja, uma falácia, as premissas podem não ser verdadeiras ou não apoiarem a conclusão.
Analise os argumentos a seguir e identifique aqueles que são falaciosos. Justifique sua resposta.
- A densidade do chumbo é de 11,30 gramas por centímetro cúbico e a do cloreto de sódio (principal componente do sal de cozinha) é de 2,17 gramas por centímetro cúbico. Para equilibrar uma balança de pratos em que de um lado foi colocado 1 centímetros de chumbo, no outro lado devem ser colocados 5 centímetros cúbicos de cloreto de sódio e mais um pouco. Isso porque, ao dividir a densidade do chumbo pela densidade do cloreto de sódio, obtém-se um valor que é maior do que 5 (11,30 ÷ 2,16 = 5,21).
- Se um cubo de gêlo de 1 centímetros cúbicos for colocado em um lado de uma balança de pratos e do outro for colocado 1centímetros cúbicos de água, conclui-se que a balança vai ficar em equilíbrio, já que se trata do mesmo material, embora em diferentes estados físicos da matéria. Isso porque a densidade é uma propriedade específica da matéria e, como trata-se do mesmo material, a densidade será a mesma e, portanto, terão a mesma massa e volume.
- Se 1 centímetros cúbicos de mercúrio a 25 graus Célsius for colocado em um lado de uma balança de pratos e do outro lado for colocado o mesmo volume de mercúrio a 50 graus Célsius, conclui-se que a balança vai ficar em equilíbrio, já que se trata do mesmo material no mesmo estado físico (líquido). Isso porque a densidade é uma propriedade específica da matéria e, como o material não se alterou, a densidade será a mesma e, portanto, terão a mesma massa e volume.
- A eletricidade que chega até as residências pode ser obtida de usinas termelétricas. Nessas usinas, o carvão mineral é transformado em outros materiais e a energia térmica liberada dessa transformação é convertida em energia elétrica. Associe cada trecho sublinhado à Física ou à Química e explique suas escolhas.
- Analise a tabela a seguir.
|
Material |
Densidade (g/cm3)* |
|---|---|
|
Chumbo |
11,30 |
|
Alumínio |
2,70 |
|
Ferro |
7,90 |
Fonte: LIDE, R. D. (edição). CRC Handbook of Chemistry and Physics. nonagésima edição(cedê- Versão 2010). Boca Raton: CRC Press/Taylor and Francis, 2009.
- Entre os materiais da tabela, qual deve ser usado para produzir um cubo de 2 centímetros de aresta com a menor massa?
- Considere dois recipientes idênticos, um deles contenha água, e o outro, com mercúrio líquido, ambos a 25 graus Célsius e ao nível do mar. Consulte a tabela “Densidade de alguns materiais” do Tema 2 e responda às questões a seguir.
- Se em cada recipiente houver o mesmo volume de cada um dos líquidos, qual recipiente conterá a maior massa? Justifique sua resposta.
- Se ambos os recipientes apresentarem a mesma massa, qual deles conterá o maior volume de material? Justifique sua resposta.
COMPARTILHAR
- Os plásticos apresentam densidades diferentes. Por exemplo, a garrafa PET tem densidade que varia entre 0,94 e 0,96 gramas por centímetro cúbico, enquanto tubos de PVC têm densidade que varia de 1,22 a 1,30 centímetros cúbicos. Nas usinas de reciclagem, os diferentes tipos de plástico precisam ser separados, já que cada um possui características próprias.
- Em grupo, façam uma pesquisa sôbre como é feita a reciclagem de plástico e elaborem uma proposta de como é possível separar uma mistura de pedaços de péti e de pê vê cê utilizando água.
- Façam e divulguem um vídeo com as informações sôbre a proposta e com atitudes visando ao uso dos recursos do planeta de maneira sustentável e consciente.
Respostas e comentários
Respostas – Atividades
1. a) Volume do paralelepípedo = 3 centímetros · 2 centímetros · 1,5 centímetro = 9 centímetros cúbicos.
b) Densidade =
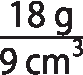
= 2 gramas por centímetro cúbico = 2.000 quilogramas por métro cúbico.
2. um. É esperado que os estudantes considerem que o argumento não é falacioso, mas eles podem contestar a imprecisão da informação sôbre a massa de cloreto de sódio utilizada. dois. Argumento falacioso. Os estudantes devem reconhecer que as densidades do gêlo e da água são distintas, logo a balança não vai ficar em equilíbrio. três. Argumento falacioso. Com o aquecimento, a densidade do mercúrio diminui. Portanto, 1 centímetro cúbico de mercúrio a 50 graus Célsius tem menor massa que o mesmo volume a 25 graus Célsius. Com isso, a balança vai pender para a amostra com a menor temperatura.
3. A transformação de energia térmica em elétrica é um fenômeno físico. Já a transformação do carvão em outros materiais é um processo químico.
4. Pelos dados apresentados, é possível determinar que todos os cubos terão o volume de 6 centímetros cúbicos. Como a densidade é a razão entre massa e volume, a massa é diretamente proporcional à densidade, logo, o metal de menor densidade vai gerar o cubo de menor massa, ou seja, o alumínio.
5. a) O recipiente com mercúrio conterá a maior massa, pois a densidade do mercúrio é maior que a da água. b) O recipiente com água conterá o maior volume, pois a densidade da água é menor que a do mercúrio.
6. Reserve um tempo para que, em grupos, elaborem a proposta solicitada. Essa é uma ótima oportunidade para aplicarem o que sabem em uma situação prática. Como o péti é menos denso que a água e o pê vê cê é mais denso, ao adicioná-la em uma mistura dêsses polímeros, eles serão separados por diferença de densidade; os fragmentos de péti devem boiar, e os de pê vê cê não. Analise os vídeos antes da divulgação e, se necessário, peça que os refaçam. Essa atividade favorece o trabalho com as competências gerais 4 e 10 da Educação Básica e as competências específicas 3, 6 e 8 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê, e com o tê cê tê – Educação Ambiental.
Versão adaptada acessível
Se necessário, realize a atividade a seguir com um colega.
Orientação para acessibilidade
Caso haja estudantes cegos ou com baixa visão na turma, oriente-os a realizar a atividade a seguir em duplas com um colega vidente.

Explore
REGISTRE EM SEU CADERNO
Construindo um instrumento para análise da densidade de líquidos
Líquidos menos densos tendem a flutuar sôbre os mais densos. Nesta atividade, veremos como é possível comparar as densidades de diferentes líquidos sem misturá-los.
Material
- Canudo de plástico
- Massa de modelar
- Caneta para marcar plástico
- 4 copos descartáveis transparentes
- Água da torneira
- Óleo de cozinha
- Mistura de água e sal de cozinha

Procedimento
- Numere os copos de 1 a 4.
- Adicione óleo de cozinha no copo 1 até a metade de sua capacidade.
- Repita o procedimento anterior para os copos 2 e 3 substituindo o óleo de cozinha por, respectivamente, mistura de água e sal de cozinha e água de torneira.
4. No copo 4, introduza

- Coloque um pouco de massa de modelar em uma das pontas do canudo plástico, que deve ficar completamente tampada. Com esse instrumento, o densímetro caseiro, é possível comparar a densidade de diferentes líquidos.
- Mergulhe o densímetro no copo 1 e marque no canudo até que ponto ele afunda no óleo.
- Repita o procedimento anterior para os copos 2 e 3. Você pode fazer marcas de cores diferentes para cada material. O canudo terá, então, uma escala com três marcas.
- Elabore uma hipótese do que irá ocorrer ao mergulhar o densímetro caseiro no copo 4.
- Introduza o densímetro no copo 4 e anote em seu caderno os resultados observados.
Analisar e discutir
- Com base nas suas observações, coloque os líquidos testados nos copos 1, 2 e 3 em ordem crescente de densidade.
- Houve diferença de densidade para os líquidos dos copos 3 e 4? Justifique sua resposta.
- Admitindo que a densidade da água da torneira no experimento é de 1 grama por centímetro cúbico, represente em seu caderno o resultado esperado ao adicionar esse densímetro no álcool de limpeza. Dado: densidade do álcool de limpeza = 0,85 grama por centímetro cúbico.
Respostas e comentários
Orientações didáticas
• Prepare a solução salina previamente, misturando de 30 gramas de sal de cozinha em 1 litro de água e a disponibilize aos estudantes.
• Auxilie-os na construção dos aparatos, fazendo adaptações quando necessário. Para aumentar a estabilidade, por exemplo, os canudos podem ser cortados; forneça tesoura com pontas arredondadas e deixe que busquem a melhor relação entre massa e comprimento.
• Ao final do experimento, convide-os a comparar seus instrumentos, a fim de que percebam as diferenças na construção e na escala e que elas não necessariamente determinam o sucesso ou o fracasso do experimento.
• Pequenas variações podem acontecer. Nesse caso, esclareça que elas comumente ocorrem durante os experimentos e são devidas, em geral, a circunstâncias não controláveis, como a manipulação do instrumento, a habilidade de observação de cada estudante e fatores próprios do equipamento, ou à variação das condições do ambiente. Se julgar conveniente, argumente que essa variações, chamadas erros não controlados, são de extrema importância para o tratamento dos dados experimentais, pois servem de parâmetro de comparação para analisar os erros controlados, que são os que realmente interessam ao experimentador.
• De acôrdo com o tempo disponível, forneça outras amostras para serem testadas, como leite e suco (tomando o cuidado de não utilizar líquidos que possam trazer risco à integridade física dos estudantes ou que produzam resíduos perigosos). Ressalte que a escala dêsse aparato não permite a determinação do valor absoluto da densidade (a menos que sejam utilizados líquidos de densidade conhecida para padronizá-lo).
• Utilize as previsões feitas na etapa 8 para avaliar as hipóteses dos estudantes, as possíveis concepções alternativas e como eles as reconstroem.
• A realização do experimento e das reflexões propostas na seção Explore permite trabalhar a competência geral 2 da Educação Básica e a competência específica 2 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê.
Respostas – Explore
1. Óleo, água da torneira e solução salina (mistura de água com sal de cozinha).
2. Sim, porque a densidade não depende da quantidade do material, mas da relação entre massa e volume.
3. O resultado esperado é que o densímetro afunde mais no álcool de limpeza do que na água, em razão da sua menor densidade.

TEMA 3 Estados físicos da matéria
A matéria pode se apresentar em diferentes estados físicos, como sólido, líquido e gasoso.
Sólido, líquido e gasoso
À temperatura de 25 graus Célsius e pressão atmosférica ao nível do mar, o ferro e o cloreto de sódio são sólidos; a água e o mercúrio são líquidos; o metano e o dióxido de carbono são gases. Como explicar essas diferenças de estado físico?
A matéria é formada por partículas muito pequenas. Em todos os estados físicos, as partículas estão em constante movimento de vibração, ou agitação térmica. A diferença entre os estados físicos ocorre no espaço existente entre as partículas do material, ou seja, na maior ou na menor agregação entre elas.
Para compreender os estados físicos da matéria, vamos utilizar o modêlo de partículas, no qual cada uma delas será representada por uma esfera colorida.
Os modelos são fórmas de representar processos ou fenômenos com o objetivo de facilitar, por exemplo, a sua visualização ou o seu entendimento. Vale ressaltar que as partículas que constituem a matéria não são esféricas nem apresentam cores, e seus tamanhos e suas proporções são diferentes dos utilizados para representá-las.
O estado sólido
Os materiais sólidos apresentam como características macroscópicasglossário o formato definido e o volume constante em determinada temperatura. Isso pode ser explicado se considerarmos que os sólidos são formados por partículas que estão vibrando bem próximas e são fortemente atraídas umas pelas outras. Alguns sólidos podem apresentar estrutura com partículas organizadas, e outros, não. Considere o esquema a seguir.
Disposições possíveis das partículas em um material sólido
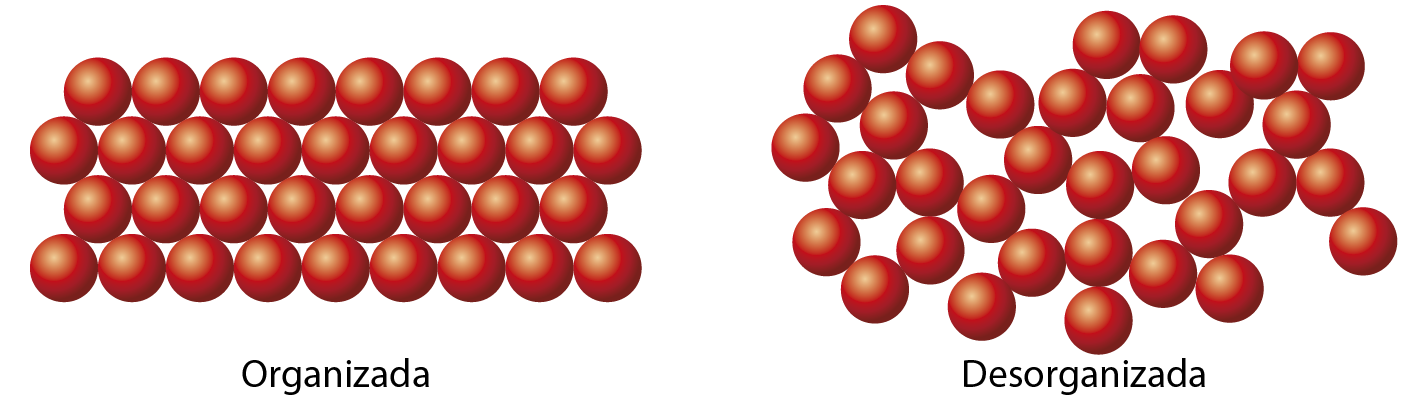
Fonte: Rrêuit, P. G. Física conceitual. décima segunda edição Porto Alegre: Bookman, 2015.
Respostas e comentários
Orientações didáticas
• Nesse momento, serão retomados e aprofundados os estudos a respeito dos estados físicos da matéria, explorando as propriedades de cada estado físico da perspectiva dos fenômenos submicroscópicos, representados por meio do modêlo de partículas. Essa abordagem mobiliza parcialmente a habilidade ê éfe zero nove cê ih zero um da Bê êne cê cê. É importante garantir que os estudantes compreendam e diferenciem fenômenos macroscópicos e submicroscópicos, e como são criados modelos e diferentes simbologias utilizadas para representar esses fenômenos. Esclareça que a maneira de representar os átomos utilizada nesta e em outras Unidades (esferas com tamanhos e cores diferentes) é apenas uma simbologia que facilita a abstração ao nível submicroscópico; quaisquer outros símbolos, no entanto, também poderiam ser utilizados, desde que bem explicados e fundamentados.
• Modelos semelhantes ao apresentado na ilustração “Disposições possíveis das partículas em um material sólido” serão utilizados frequentemente para indicar as partículas de vários materiais. Ressalte que esse modêlo é uma representação das partículas submicroscópicas e tem como objetivo facilitar sua visualização e o desenvolvimento de novas ideias pelos estudantes. Deve ficar claro para a turma que mesmo um modêlo não sendo uma representação fiel da realidade, ele é muito útil, pois facilita a visualização de processos, ideias e eventos que são muito abstratos – é o caso das diferentes interações que regem os estados físicos da matéria. Comente que essa limitação não invalida o uso dos modelos, pois eles são empregados pelos cientistas na produção do conhecimento, para testar ou refutar suas hipóteses, além de serem aperfeiçoados à medida que novos resultados experimentais são obtidos.
Confira a seguir algumas propriedades específicas observáveis nos sólidos.
Dureza é a propriedade relacionada à capacidade de riscar e ser riscado. Quanto mais duro for um sólido, mais difícil é riscar sua superfície. Isso acontece quando as partículas se agrupam de maneira muito próxima e organizada na estrutura do sólido, como no diamante, que é empregado em diversas aplicações por conta dessa propriedade. Ele pode ser lapidado a fim de ser usado para cortar ferro e aço, serrar pedras, polir, moer e raspar diferentes tipos de instrumento.

A ductibilidade e a maleabilidade estão relacionadas com a capacidade que alguns sólidos apresentam de se deformar e não recuperar formato original quando a força causadora da deformação cessa. Isso é possível porque as partículas não formam estruturas tão organizadas.

A elasticidade é característica dos sólidos que se deformam, mas recuperam o formato original quando cessa a força causadora da deformação. Se a força aplicada é maior que a força de interação entre as partículas que formam o material, então ele se rompe e não volta ao seu formato original.

Resistência ou tenacidade é a propriedade dos materiais relacionada com sua capacidade de suportar forças externas sem se romper ou se fraturar. Um corpo sólido formado por ferro é mais resistente do que um formado por argila.

Respostas e comentários
Orientações didáticas
• Trabalhe cada uma das propriedades dando exemplos de materiais que estejam presentes no cotidiano dos estudantes. Comente a diferença entre diamante e brilhante; o primeiro se trata de uma pedra encontrada na natureza e o segundo é um tipo de lapidação do diamante (e também de outras gemas), comumente utilizado em joias. Enfatize a importância de se conhecer as propriedades dos materiais para selecionar aqueles mais adequados a cada função. Caso julgue pertinente, comente a respeito dos materiais compósitos, que são combinações de materiais diferentes, com o objetivo de obter um material com propriedades distintas das originais. O texto indicado na Sugestão de recurso complementar trata dêsse assunto.
• Se julgar oportuno, solicite que os estudantes realizem, como tarefa de casa, a leitura do Tema 3 e elaborem um mapa conceitual apresentando os principais conceitos apresentados no texto. No dia da aula sôbre o assunto, peça a alguns estudantes que apresentem seus mapas conceituais para a turma. Tire as dúvidas que surgirem, solicite aos estudantes que realizem os ajustes necessários e exponha os mapas produzidos na sala para auxiliar no desenvolvimento do Tema. Essa mesma prática pode ser realizada para cada um dos estados físicos apresentados no material.
Sugestão de recurso complementar
Artigo
BIZETO, M. A. A inspiração que vem da natureza, Portal do Conselho Regional de Química – quatro Região, 2011.
O texto aborda conceitos como material híbrido, compósitos e nanocompósitos.
Disponível em: https://oeds.link/WfahVs. Acesso em: 11 agosto 2022.
O estado líquido
Os líquidos apresentam, em determinada temperatura, volume constante e partículas mais afastadas umas das outras que as dos sólidos, pois a atração entre elas é menor, permitindo que vibrem mais intensamente e se desloquem. Como nesse caso as partículas apresentam maior liberdade de movimentação que as dos sólidos, os líquidos adquirem o formato do recipiente que os contém.

Fonte: Rrêuit, P. G. Física conceitual. décima segunda ediçãoPorto Alegre: Bookman, 2015.
O modêlo de partículas também ajuda a explicar duas propriedades específicas facilmente observáveis nos líquidos: a volatilidade e a viscosidade.
A volatilidade de um material está associada à facilidade com que ele evapora.
À temperatura de 25 graus Célsius e à pressão atmosférica ao nível do mar, o éter, a acetona e o etanol são líquidos mais voláteis que a água. Isso significa, entre outros fatores, que a fôrça de atração entre as partículas do éter, da acetona e do etanol é menor que a fôrça de atração entre as partículas da água. Dessa fórma, esses materiais evaporam mais facilmente que a água. A volatilidade torna-se maior com o aumento da temperatura.

A viscosidade está relacionada com a resistência que um material oferece ao escoamento. Simplificadamente, líquidos com forte atração entre suas partículas apresentam maior viscosidade. À temperatura de 25 graus Célsius e ao nível do mar, o óleo lubrificante e o mel apresentam viscosidade elevada em comparação com a água. Portanto, a água escoa mais facilmente que esses materiais.


Vamos fazer
REGISTRE EM SEU CADERNO
O volume dos gases pode ser alterado?
Material
• 1 saco plástico de lixo na côr preta
Procedimento
- Abra o saco de lixo para que entre ar nele. Certifique-se de que não esteja furado.
- Feche-o muito bem, formando uma bolsa de ar, e deixe-o exposto ao Sol.
Analisar e concluir
- O que você espera que aconteça?
- Depois de algumas horas, o que ocorreu com o saco de lixo? Por quê? O resultado está de acôrdo com sua hipótese inicial?
- Compare sua conclusão com a dos colegas. Há diferenças? Por quê?
Respostas e comentários
Orientações didáticas
• Na caracterização do estado líquido, são discutidos os conceitos de volatilidade e de viscosidade. Ressalte que a volatilidade do líquido está relacionada à atração entre suas partículas e à massa dessas partículas. Caso partículas de massas semelhantes estejam unidas com forças de atração intensas, o líquido tende a ser menos volátil. Portanto, a volatilidade pode ser usada para introduzir as características do estado gasoso. Com a evaporação, ocorre a separação das partículas, e o líquido se transforma em vapor. Peça aos estudantes que comparem as ilustrações do modêlo de partículas para os estados líquido e gasoso (mais adiante) mostradas no livro do estudante, favorecendo a mobilização da habilidade ê éfe zero nove cê ih zero um da Bê êne cê cê.
• Com base na imagem mostrando um difusor de óleos essenciais (aromatizador de ambiente), destaque o efeito da temperatura sôbre a volatilidade das substâncias, retomando o conceito submicroscópico, como previsto pela habilidade ê éfe zero nove cê ih zero um da Bê êne cê cê.
• Exemplifique a viscosidade com materiais do cotidiano dos estudantes, como mel, óleo lubrificante e azeite. Para eliminar a concepção equivocada de que materiais mais viscosos são também mais densos, cite o exemplo do óleo e da água, em que o óleo é mais viscoso, porém menos denso que a água. Esclareça que a viscosidade também é uma característica dos gases.
• Ao realizar os procedimentos descritos na seção Vamos fazer, certifique-se de que os sacos foram fechados adequadamente. Estimule os estudantes a refletir sôbre sua ideia inicial com base no resultado obtido na atividade prática e a comunicar suas conclusões para a turma. A autoavaliação e a reformulação de hipóteses são muito importantes, pois se trata de processos por meio dos quais os estudantes analisam a metodologia utilizada e refletem sôbre ela. Essa abordagem favorece o desenvolvimento da competência geral 2 da Educação Básica e da competência específica 2 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê.
Respostas – Vamos fazer
1. Resposta pessoal. Instrua-os a anotar suas hipóteses para serem confrontadas posteriormente.
2. Após certo tempo sob o Sol, o volume do ar contido no saco aumentará em decorrência da elevação da temperatura, que aumenta a agitação das partículas, desencadeando maior ocupação de espaço do que no início do experimento.
3. Resposta pessoal. Oriente-os a ouvir os colegas respeitando a opinião de cada um e exponha as conclusões na lousa, para que seja mais fácil comparar as diferenças.
O estado gasoso
Os gases têm formato e volume variáveis que dependem do recipiente que os contém. Eles ocupam todo o espaço disponível; assim, se a capacidade do recipiente aumenta, eles se expandem; se a capacidade diminui, eles se comprimem. Na imagem, o gás, comprimido no tanque, se expande ao encher o balão de festa.
De acôrdo com o modêlo de partículas, nos gases, as partículas estão desorganizadas e muito afastadas umas das outras. A fôrça de atração entre elas possui intensidade pequena; dêsse modo, as partículas de um gás têm grande liberdade de movimento, mantendo-se mais distantes umas das outras que nos líquidos e nos sólidos. Por isso, os gases podem ser expandidos ou comprimidos. Nesta etapa do estudo dos materiais, considere os termos “gás” e “vapor” equivalentes.

Fonte: Rrêuit, P. G. Física conceitual. décima segunda ediçãoPorto Alegre: Bookman, 2015.
De ôlho no tema
Na imagem, o ilustrador procurou representar os estados físicos da matéria. Note que, por se tratar de uma ilustração de caráter artístico, ela não apresenta rigor teórico.
- O ilustrador fez uso de um recurso de humor na composição. Qual foi o entendimento dele sôbre o termo "estado"? Justifique sua resposta usando elementos da imagem.
- Descreva quais elementos da natureza o artista utilizou para representar cada um dos estados físicos da matéria.
- Explique as diferenças entre os estados físicos da matéria com base nas suas características macroscópicas.

Respostas e comentários
Orientações didáticas
• Se julgar oportuno, extrapole o resultado da atividade da seção Vamos fazer para explicar o funcionamento dos balões de ar quente. Fazendo uso do modêlo de partículas, mostre que as partículas que compõem o ar aquecido pelo maçarico passam a se movimentar de maneira mais agitada, ocorrendo maior separação entre elas. Como parte do ar frio escapa para fóra do balão, a porção de ar quente que fica ocupa todo o espaço interno do balão e o torna menos denso que o ar, possibilitando sua subida. Portanto, na atividade da seção Vamos fazer e no exemplo do balão é analisada a influência da temperatura sôbre a densidade dos gases.
Respostas – De ôlho no tema
a) O termo “estado” remete ao sentido geográfico, reforçado pela presença da rosa dos ventos e pela divisão com fios contínuos e tracejados, característica de mapas presentes na ilustração.
b) O artista utilizou elementos da natureza como rios, montanhas cobertas com neve e vapor para representar os estados físicos líquido, sólido e gasoso, respectivamente.
c) Os sólidos apresentam volume e formato definidos; os líquidos apresentam volume definido pelo formato do recipiente que os contém; e os gases têm formato e volume variáveis, ocupando todo o espaço do recipiente em que eles se encontram.
• Esse exercício de leitura inferencial de imagem integra duas fontes de informação: o conhecimento prévio acerca dos estados físicos da matéria e a informação visual, a obra em si.

Tema 4
Mudanças de estado físico
A variação da temperatura pode provocar mudanças de estado físico da matéria.
A temperatura é a grandeza que indica o grau de agitação das partículas da matéria. Quanto maior a intensidade da agitação das partículas, maior é a temperatura de um corpo.
Corpos com temperaturas diferentes, quando em contato, sempre trocam energia térmica. Calor é o nome dado à energia transferida em razão da diferença de temperatura entre dois corpos. Essa troca sempre ocorre do corpo de maior temperatura para o de menor temperatura.
A influência da temperatura
O estado físico de um corpo depende da temperatura e da pressão a que ele está submetido.
Para que um corpo mude de estado físico, é necessário alterar a intensidade da agitação de suas partículas, o que pode ser feito mudando a pressão ou, de maneira mais comum, fornecendo ou retirando energia térmica do corpo. Dessa fórma, tanto o aumento como a diminuição da temperatura podem provocar transformações nos estados físicos da matéria.
Mudanças de estado físico da água
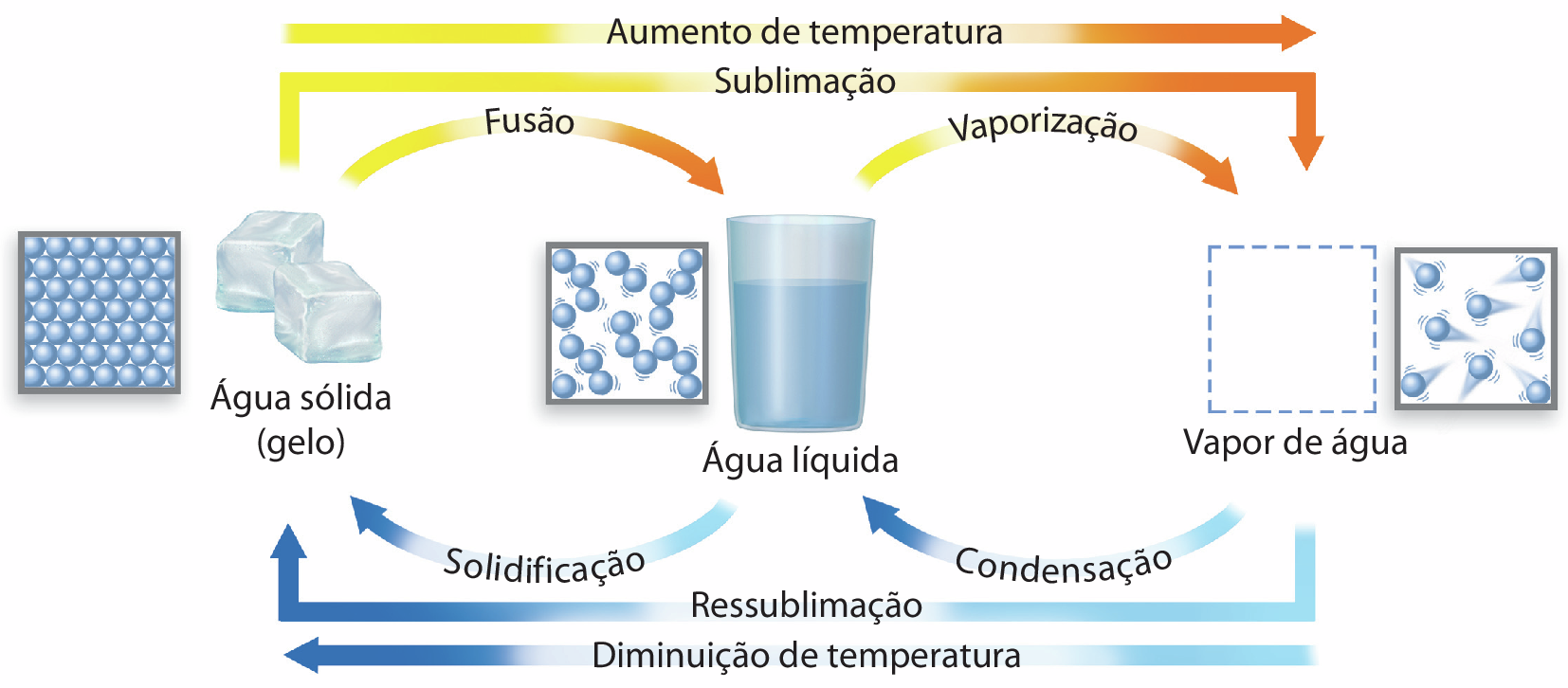
Fonte: Rrêuit, P. G. Física conceitual. décima segunda edição Porto Alegre: Bookman, 2015.
Entrando na rede
Na página do PhET Interactive Simulations, disponível em: https://oeds.link/BkqMIy há um simulador que pode ajudá-lo a compreender o que ocorre nas mudanças de estado físico da matéria.
Acesso em: 7 agosto 2022.
Respostas e comentários
Orientações didáticas
• As mudanças de estado físico são discutidas pela abordagem da transferência de calor e mudança de temperatura. Dessa fórma, retome os conhecimentos prévios dos estudantes sôbre esses conceitos, trabalhados no 7º ano, pois são pré-requisitos para a compreensão sôbre as mudanças de estado físico.
• Neste Tema, pode ser aplicada a Oficina 1 – Mudanças de estado físico, no momento que considerar mais propício.
• No início do estudo deste Tema, retome os exemplos trabalhados no Tema 3: o efeito da vela na dissipação do aroma dos óleos essenciais e o efeito do calor do Sol no saco plástico contendo ar. Questione os estudantes sôbre o que esses dois exemplos têm em comum. Espera-se que eles destaquem o calor como uma variável comum às duas situações.
• Uma ideia muito comum que os estudantes apresentam é a de que existe troca tanto de calor quanto de frio. Essa ideia está inserida em algumas concepções equivocadas a respeito do conceito de calor e temperatura. Para auxiliá-los na ressignificação dêsses conceitos, recorra ao texto indicado na Sugestão de recurso complementar, que discute as concepções a níveis macro e microscópicos que os estudantes apresentam.
• Trabalhe a imagem “Mudanças de estado físico da água”, auxiliando os estudantes a entenderem as relações entre as mudanças físicas macroscópicas e submicroscópicas, favorecendo o desenvolvimento da habilidade ê éfe zero nove cê ih zero um da Bê êne cê cê. Caso julgue relevante, associe o esquema ao ciclo da água no ambiente, relembrando sua importância para a manutenção da vida na Terra.
Sugestão de recurso complementar
Artigo
MORTIMER, E. F.; AMARAL, L. O. F. Quanto mais quente melhor: Calor e temperatura no ensino de termoquímica. Química Nova na Escola, número7, página 30-34, 1998.
O artigo apresenta concepções prévias de estudantes em relação aos conceitos de calor e temperatura.
Disponível em: https://oeds.link/CjBw16. Acesso em: 12 agosto 2022.
Mudanças que ocorrem com o aumento da temperatura
As mudanças de estado físico que ocorrem com o aumento da temperatura são: fusão, vaporização e sublimação.
Fusão é a mudança do estado sólido para o estado líquido. Ocorre, por exemplo, na indústria metalúrgica quando os metais são fundidos.
Vaporização é a mudança do estado líquido para o estado gasoso. Essa transformação pode ocorrer de duas maneiras distintas: pela evaporação e pela ebulição.
- Evaporação é um processo que ocorre de fórma lenta, principalmente na superfície do líquido, sem o surgimento de bolhas. Um exemplo é quando a água da roupa molhada no varal evapora.
- Ebulição é um processo rápido que ocorre em todas as partes do líquido, com formação de bolhas de vapor. Quando isso acontece, dizemos que o líquido está fervendo.
Sublimação é a mudança direta do estado sólido para o estado gasoso, sem passar pelo estado líquido. É observada facilmente no caso de alguns sólidos constituídos por um material que sublima à pressão ambiente, como o gêlo-sêco, que é o gás carbônico em estado sólido, a temperatura inferior a –78 graus Célsius.

Mudanças que ocorrem com a diminuição da temperatura
A diminuição da temperatura pode provocar a condensação, a solidificação e a ressublimação.
Condensação é a mudança do estado gasoso para o estado líquido. Por exemplo, o vapor de água que existe em nossa respiração condensa-se quando é esfriado. Observamos essa condensação quando expiramos em um dia frio e vemos formar a névoa branca que sai de nossa boca.
Solidificação é a mudança do estado líquido para o estado sólido. Por exemplo, quando a água líquida transforma-se em gêlo ao ser colocada no congelador.
Ressublimação é a mudança do estado gasoso diretamente para o estado sólido. Algumas substâncias que podem ressublimar à pressão ambiente são o iodo e a naftalina.

Temperatura de fusão e temperatura de ebulição
A temperatura de fusão é aquela em que ocorre a mudança do estado sólido para o líquido e equivale à temperatura de solidificação. A temperatura de fusão da água “pura”, ao nível do mar, é 0 grau Célsius. Nesse caso, água “pura” é aquela que não tem nenhum outro material dissolvido nela. Do início ao fim da fusão de determinada quantidade de água pura, essa temperatura não se altera.
A temperatura de ebulição é aquela em que ocorre a mudança do estado líquido para o gasoso e equivale à temperatura de condensação. A temperatura de ebulição da água “pura”, ao nível do mar, é 100 graus Célsius.
Respostas e comentários
Orientações didáticas
• Ao mencionar a fundição dos metais sob altas temperaturas, explique que alguns dêsses materiais, como o mercúrio, podem se apresentar no estado líquido à temperatura ambiente e à pressão atmosférica ao nível do mar.
• A condensação pode ser observada quando, num dia muito frio, a superfície interna de uma janela fica embaçada ou quando se retira uma garrafa de água da geladeira e ela fica úmida. Na superfície oposta à que está em contato com o frio (ou seja, o lado de dentro da janela ou o lado de fóra da garrafa de água) vai se formar uma camada de gotículas de água. As gotículas são provenientes da condensação do vapor de água, que, em razão da diminuição de temperatura, retornou ao estado líquido.
• Ao abordar os diferentes exemplos de mudança de estado físico, recorra ao modêlo de partículas, de modo que os estudantes relacionem os aspectos macroscópicos ao estado de agitação e organização das partículas, favorecendo o trabalho com a habilidade ê éfe zero nove cê ih zero um da Bê êne cê cê. Para auxiliá-los nesta abordagem, é possível explorar o simulador indicado no quadro Entrando na rede.
Sugestão de recurso complementar
Material de apôio
, M. J. C. Caderno pedagógico de atividades práticas e experimentais para uma aprendizagem significativa de conceitos físicos em Ciências. Bandeirantes: Universidade Estadual do Paraná, 2008.
O caderno apresenta atividades práticas com materiais acessíveis que contribuem para o aprendizado significativo dos estudantes.
Disponível em: https://oeds.link/rTv7zi. Acesso em: 7 julho 2022.
As temperaturas de fusão e de ebulição são propriedades específicas da matéria que podem ser usadas para identificar diferentes materiais. Por exemplo, para diferenciar sólidos visualmente semelhantes como o cloreto de sódio (principal componente do sal de cozinha) e o carbonato de sódio (utilizado na fabricação do vidro), verificamos, ao nível do mar, a temperatura de fusão do cloreto de sódio, que é 801 graus Célsius, e a do carbonato de sódio, que é 851 graus Célsius.
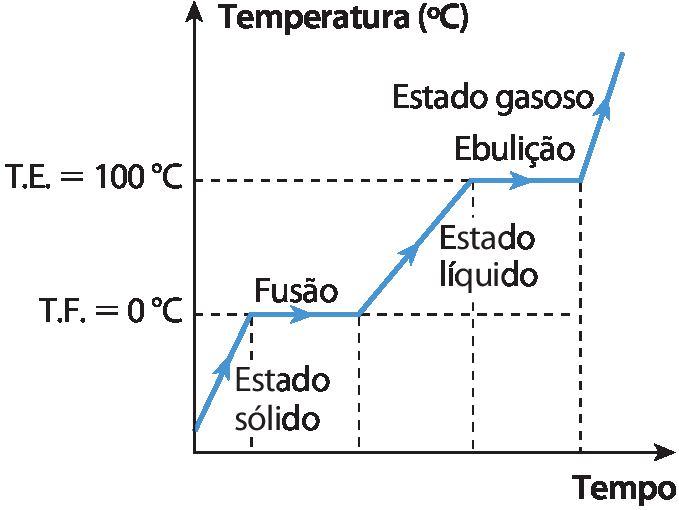
Os gráficos a seguir representam as mudanças de estado físico da água pura, ao nível do mar, em processo de aquecimento e de resfriamento.
Aquecimento da água pura (ao nível do mar)
Resfriamento da água pura (ao nível do mar)
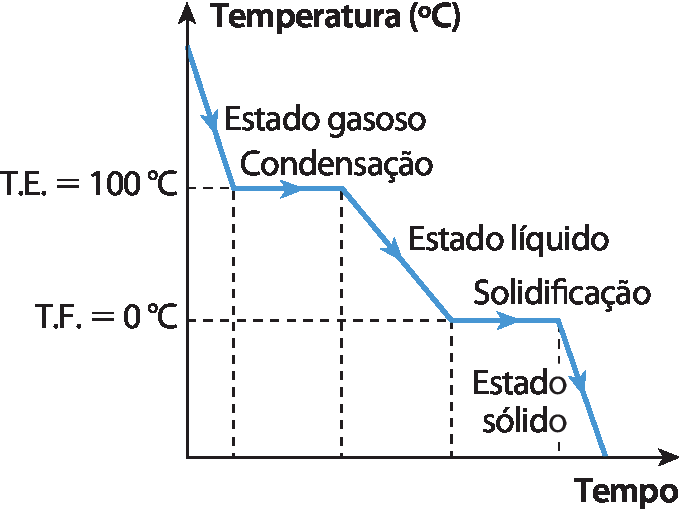
Fonte: Gráficos elaborados com base em LIDE, R. D. (edição). CRC Handbook of Chemistry and Physics. nonagésima edição (cêdê- Versão 2010). Boca Raton: CRC Press/Taylor and Francis, 2009.

Vamos fazer
REGISTRE EM SEU CADERNO
Líquidos distintos solidificam-se a temperaturas diferentes?
Material
- 2 copos descartáveis de plástico
- Copo medidor
- 200 mililitros de água da torneira
- 200 mililitros de álcool 40%
- Congelador de uma geladeira
- 2 pedaços de fita-crepe e caneta
ATENÇÃO
Apesar de o álcool 40% ser comercializado em muitos estabelecimentos tanto na fórma de gel quanto na fórma líquida, ele pode entrar em combustão se levado próximo a uma fonte de calor. Certifique-se de que não haja fontes de calor próximas ao álcool 40% durante a realização da atividade. Não ingerir esse produto.
Procedimento
- Com o auxílio do copo medidor, coléte 200 mililitros de água da torneira.
- Transfira a água para um copo de plástico e identifique-o com a fita-crepe e a caneta.
- Com o copo medidor sêco, coléte 200 mililitros de álcool 40%.
- Transfira o álcool para outro copo de plástico e identifique-o.
- Coloque os copos no congelador.
- Espere no mínimo 24 horas para observar o aspecto dos líquidos.
Analisar e explicar
- Quanto tempo você deixou os copos descartáveis no congelador? Ao final dêsse tempo, algum dos líquidos mudou de estado físico? Se sim, qual ou quais?
- Faça uma pesquisa e identifique as temperaturas de fusão da água e do álcool 40%. Sabendo que a temperatura alcançada por congeladores domésticos está aproximadamente entre –15 graus Célsius e –20 graus Célsius, as informações obtidas na pesquisa são coerentes com o resultado da atividade?
Respostas e comentários
Orientações didáticas
• A fim de tornar mais claro o conceito de temperatura de ebulição diante do fenômeno de evaporação, proponha as seguintes questões aos estudantes: “Por que as roupas molhadas secam quando estendidas no varal?” e “A água atinge 100 graus Célsius quando exposta ao Sol?”. Esclareça que a ebulição é decorrente do aquecimento até que o material atinja uma temperatura específica (temperatura de ebulição); a evaporação ocorre em baixa velocidade e é um processo que depende da volatilidade do material e das condições ambientes (temperatura, umidade do ar, incidência de vento etcétera).
• Os gráficos “Aquecimento da água pura (ao nível do mar)” e “Resfriamento da água pura (ao nível do mar)” auxiliam os estudantes a entender a variação da temperatura da água nos diferentes estados físicos e como a temperatura se comporta durante a mudança de estado físico. As várias inclinações se devem às diferenças de calor específico da água nos três estados físicos representados, além do calor latente de fusão e de vaporização. Neste nível de ensino, é suficiente comentar com os estudantes que a transferência de calor acontece de maneira diferente para cada estado físico, já que a agregação das partículas em cada estado muda.
• Para a atividade proposta na seção Vamos fazer, certifique-se de que a água e o álcool estejam inicialmente à temperatura ambiente. Apesar de a água solidificar-se após algumas horas no congelador, o objetivo de observar os resultados após 24 horas é para que os estudantes não considerem que o álcool 40% não congelou porque ficou tempo insuficiente no congelador. Estimule-os a registrar suas descobertas e a comparar seus resultados. Explore as características dos materiais questionando aos estudantes se seria possível identificar a água e o álcool sem resfriá-los e caso os copos não estivessem identificados. Para o mesmo volume de água e de álcool, medindo a massa e pesquisando o valor da densidade dêsses materiais, pode-se verificar que o álcool é menos denso, portanto o copo com álcool 40% terá massa menor. A atividade auxilia no desenvolvimento da competência específica 3 de Ciências da Natureza para o Ensino Fundamental, prevista pela Bê êne cê cê.
Respostas – Vamos fazer
1. Resposta pessoal. Espera-se que os copos sejam deixados pelo menos 24 horas no congelador. Esse tempo é suficiente para garantir o congelamento da água da torneira e evidenciar que o álcool 40% não congela a essa temperatura. Espera-se que apenas a água da torneira tenha mudado para o estado sólido.
2. Ao nível do mar, a água da torneira funde a aproximadamente 0 grau Célsius. Nas mesmas condições, o álcool 40% funde a –118 grau Célsius, muito abaixo da temperatura do congelador, o que é coerente com os resultados esperados da atividade.
A influência da pressão
Além da temperatura, a pressão também influencia as mudanças de estado físico.
Vamos utilizar a água pura para exemplificar o efeito da pressão nas mudanças de estado físico.
A pressão atmosférica diminui à medida que aumenta a altitude. Na tabela a seguir, apresentamos os valores aproximados da altitude de três municípios em relação ao nível do mar, da pressão atmosférica nesses locais e das respectivas temperaturas de ebulição da água pura.
|
Local |
Altitude em relação ao nível do mar (m) |
Pressão atmosférica aproximada (atm) |
Temperatura aproximada de ebulição da água (°C) |
|---|---|---|---|
|
Rio de Janeiro |
0 |
1,00 |
100 |
|
São Paulo |
760 |
0,92 |
98 |
|
Brasília |
1.200 |
0,86 |
96 |
*Valores aproximados de altitude, pressão atmosférica e temperatura de ebulição da água. A pressão de 1 atmosfera (1 a tê eme) equivale a 101325 Pa (pascal). O pascal é a unidade de pressão no SI.
Fontes: INSTITUTO BRASILEIRO DE GEOGRAFIA E ESTATÍSTICA. Anuário estatístico do Brasil. volume 77. Rio de Janeiro: IBGE, 2017. Disponível em: https://oeds.link/3aZM3t EARL, B. L. The direct relation between altitude and boiling point. Journal of Chemical Education. volume 67 (1). 1990. Disponível em: https://oeds.link/sXEvAo. Acessos em: 7 agosto 2022.
Note, com base nos dados dessa tabela, que as variações da altitude estão relacionadas às mudanças nos valores de temperatura de ebulição da água.
Saiba mais!
COMO FUNCIONA A PANELA DE PRESSÃO?
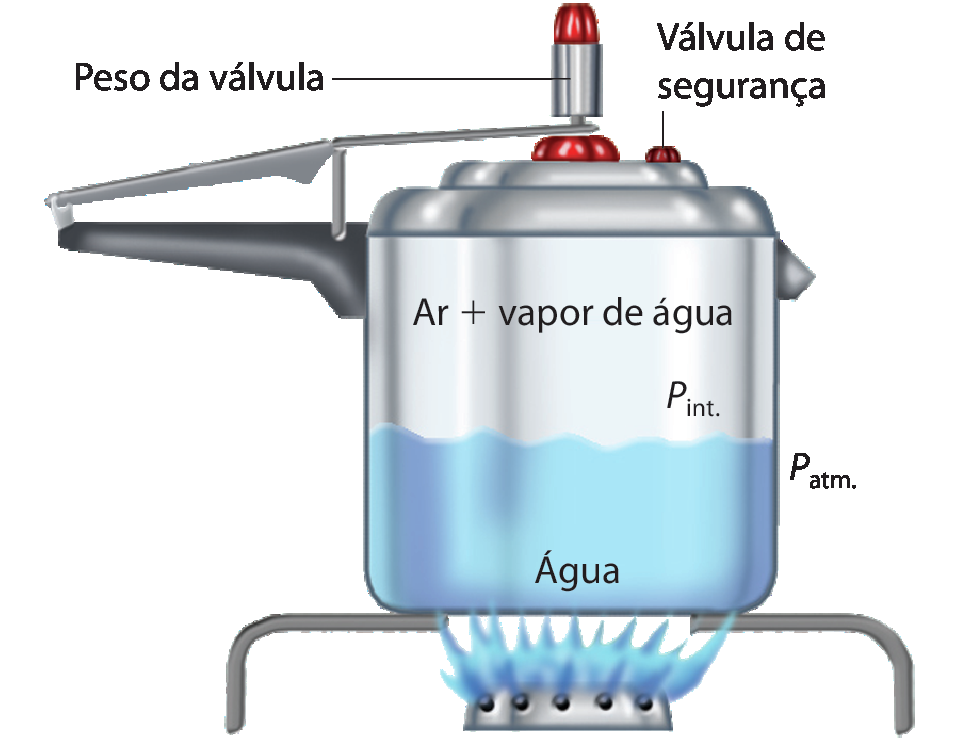
Os alimentos cozinham mais rapidamente na panela de pressão porque eles atingem temperaturas maiores do que em uma panela comum. Dentro da panela, sob maior pressão – a pressão interna (pê) é maior que a pressão atmosférica (pê) –, a temperatura de ebulição ultrapassa os 110 graus Célsius. Nesse tipo de panela, o vapor formado só pode escapar por um orifício central na tampa, sôbre o qual se assenta uma válvula. Com o aumento da pressão, o pêso é levantado, liberando vapor e equilibrando a pressão interna. Se não houvesse a válvula de escape, o aumento da pressão faria a panela explodir. Dessa fórma, para utilizar uma panela de pressão de maneira segura, é necessário limpar regularmente a válvula de segurança, os orifícios do pêso da válvula e respeitar o volume máximo suportado pela panela.
Funcionamento de uma panela de pressão
De ôlho no tema
Na natureza, a água passa por diferentes mudanças de estado físico.
- Qual é o termo utilizado para descrever o derretimento das geleiras em água líquida?
- E para descrever a mudança de estado físico da água dos rios que vira vapor?
- O que significa dizer que o gêlo sublimou?
- Considere um aparato de vidro, constituído por dois bulbos ligados por um tubo, totalmente vedado e contendo um pouco de álcool. Se você segurar esse aparato com as mãos pela na parte de baixo, o que deve acontecer?

Respostas e comentários
Orientações didáticas
• Peça aos estudantes que interpretem a tabela que apresenta a pressão atmosférica e a temperatura de ebulição da água em diferentes locais. Auxilie-os a relacionar a altitude do município em relação ao nível do mar, a pressão atmosférica e a temperatura de ebulição da água. Explique o comportamento das partículas que constituem a água em diferentes altitudes e como isso interfere na temperatura de ebulição. Esclareça que a pressão atmosférica de determinado local não é constante e pode se alterar, por exemplo, com as variações climáticas causadas pela movimentação das massas de ar. Uma atmosfera (1 a tê eme) é a pressão que a atmosfera terrestre exerce ao nível do mar.
• Explicite o funcionamento da panela de pressão, mostrando por que ela torna o cozimento dos alimentos mais rápido. Aproveite para discutir questões relacionadas à segurança, como verificar se a válvula não tem nenhuma obstrução antes de usar a panela, não mexer na válvula durante o cozimento dos alimentos e esperar que a pressão interna diminua para abri-la após o seu uso.
Respostas – De ôlho no tema
a) Fusão.
b) Vaporização.
c) Significa que a água passou diretamente do estado sólido para o estado gasoso, sem passar pelo estado líquido.
d) Ao encostar a mão na parte de baixo do aparato, o gás contido se aquece e expande. Com o aumento da pressão, o álcool sobe. Esse aparato é conhecido por ebulidor de Franklin.

Atividades
TEMAS 3 E 4
REGISTRE EM SEU CADERNO
ORGANIZAR
- Um material pode apresentar diferentes propriedades dependendo do estado físico em que se encontra. Determine qual estado físico (sólido, líquido ou gasoso) está relacionado às situações descritas a seguir.
- Ar comprimindo-se dentro de uma seringa tampada quando o êmbolo é empurrado para dentro.
- Parafina derretida sendo despejada em uma fórma para fazer vela.
- Diamante sendo usado para cortar metais como o ferro.
- Com base no modêlo de partículas, explique os fatos a seguir.
- O vapor de água, com a diminuição da temperatura, transforma-se em água líquida.
- Ao abrir um frasco com perfume, mesmo a certa distância, percebe-se rapidamente sua fragrância.
ANALISAR
3. As figuras A e B representam o mesmo gás em duas temperaturas diferentes. Os vetores representam a intensidade, o sentido e a direção da velocidade das partículas. Quanto maior o comprimento dos vetores, maior é a agitação das partículas.
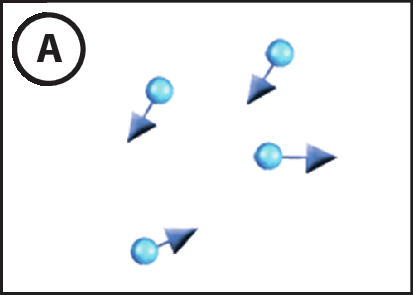
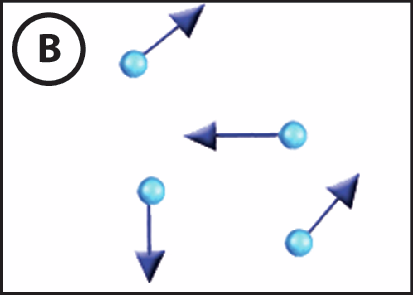
- Qual das figuras, A ou B, representa o gás com maior temperatura? Justifique sua resposta.
- A naftalina é comercializada como inseticida na fórma de esferas sólidas que diminuem de tamanho com o passar do tempo. O vapor de naftalina é nocivo tanto para os insetos como para os humanos; por isso, ela sempre deve ser utilizada conforme a indicação do fabricante.
- Qual é a mudança de estado físico que justifica a diminuição do tamanho da esfera de naftalina com o passar do tempo?
- Consulte a tabela “Pressão atmosférica e temperatura de ebulição da água em alguns locais” para responder às questões a seguir.
- Considerando chamas com a mesma intensidade e amostras de água com o mesmo volume e a mesma temperatura inicial, em qual cidade, Rio de Janeiro ou Brasília, a água entrará em ebulição mais rapidamente? Responda com um argumento científico contendo os elementos: dado, conclusão, qualificador, apôio, garantia e refutador.
- Se nessas duas cidades forem usadas panelas de pressão para aquecer a água, o tempo para que a água pura entre em ebulição será diferente? Justifique sua resposta.
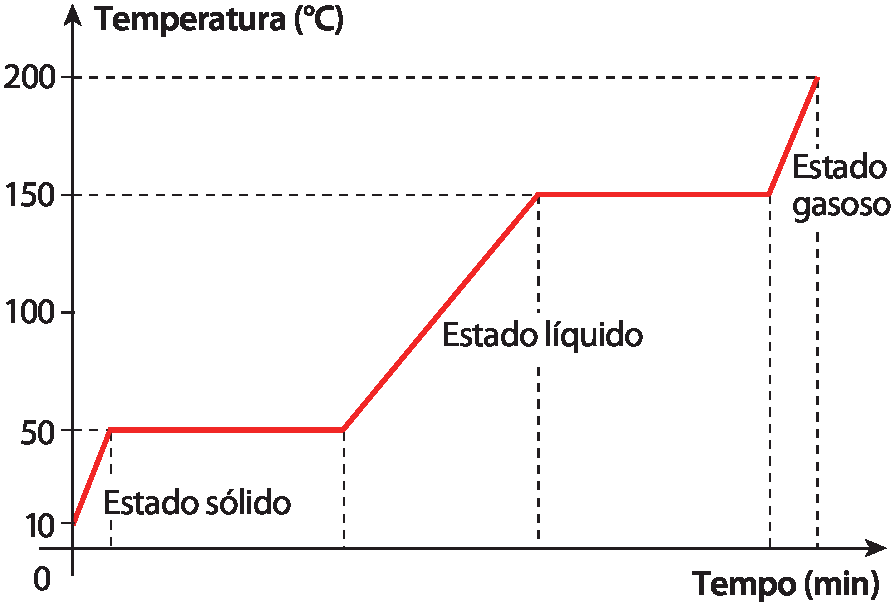
- Considere o gráfico a seguir.
- Quais são as temperaturas de fusão e de ebulição do material? Explique sua conclusão.
Curva de aquecimento de determinado material
COMPARTILHAR
7. A liofilização é um processo empregado pela indústria alimentícia na desidratação de alguns alimentos. Em grupo, pesquisem sôbre esse processo em fontes confiáveis. Identifiquem quais passagens de estados físicos ocorrem na liofilização e como elas são feitas. Informem-se sôbre outros tipos de indústria que também utilizam a liofilização. Reúnam todas as informações obtidas em um mural composto de imagens e pequenos textos e o exponham em sua escola, nas redes sociais, em blogs e em outras mídias, após aprovação do professor.
Respostas e comentários
Respostas – Atividades
1. a) Estado gasoso. b) Estado líquido. c) Estado sólido.
2. a) A diminuição da temperatura é resultado da diminuição da movimentação das partículas, que se aproximam umas das outras, aumentando a fôrça de atração entre elas. b) Com o frasco aberto, o perfume pode passar do estado líquido para o estado gasoso, e, nesse estado, as partículas preenchem todo o espaço disponível. Assim, as partículas constituintes do perfume alcançam lugares distantes difundindo-se pelo espaço.
3. Figura B. Quanto maior a temperatura de um corpo, maior é a movimentação de suas partículas; nesse caso, representada na ilustração pelos vetores mais compridos.
4. Sublimação.
5. a) Esta é a primeira vez que o elemento refutador aparece nas atividades argumentativas do livro, por isso é importante dar-lhe destaque e auxiliar os estudantes.
Dado que a intensidade da chama é a mesma, assim como a temperatura inicial da água, conclui-se que a água provavelmente (qualificador) entrará em ebulição primeiro em São Paulo, já que (garantia) a cidade do Rio de Janeiro está ao nível do mar, enquanto São Paulo está a 760 métro de altitude. Isso porque (apôio) a pressão atmosférica diminui à medida que aumenta a altitude e, quanto menor a pressão atmosférica, menor a temperatura de ebulição da água. Esse resultado é esperado, a não ser que (refutador) as amostras não sejam idênticas, se houver materiais dissolvidos diferentes isso pode fazer variar a temperatura de ebulição das amostras. b) Não, pois no interior dêsse tipo de panela a pressão não depende da pressão atmosférica.
6. A temperatura de fusão é 50 graus Célsius, e a de ebulição, 150 graus Célsius. As temperaturas de transição de fase são representadas por um patamar constante em um intervalo de tempo.
7. A liofilização é um processo de desidratação empregado para aumentar a durabilidade dos alimentos. Nele, o alimento é congelado e depois submetido ao vácuo, o que facilita a sublimação da água. Com isso, a água congelada passa diretamente para o estado gasoso, sem alterar as propriedades nutritivas do alimento. Essa atividade favorece o trabalho com a competência geral 5 da Educação Básica e com a competência específica 6 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê.

Pensar Ciência
A luta de uma cientista
Uma das mais importantes cientistas do século vinte foi a química e biofísica inglesa Frânclin (1920-1958). , com suas pesquisas nos anos 1940 e 1950, foi pioneira na compreensão do formato e do funcionamento da molécula de dê êne á, chegando a antecipar algumas concepções do inglês frêncis cric e do estadunidense Djeimes Uatson, considerados os “pais” do dê êne á.
Desde o princípio, sofreu oposição à sua carreira. Seu pai não aceitava que uma mulher tivesse formação acadêmica. Por causa da mentalidade da sociedade da época, mulheres não eram bem-vistas nas áreas das Ciências. Assim, para despontar na carreira científica, ela teve de enfrentar a resistência da sociedade e de colegas cientistas.
e Morrice Uilkinsreceberam, em 1962, o Prêmio Nobel por seus trabalhos com a molécula de dê êne á. , que havia morrido de câncer no ovário quatro anos antes, aos 37 anos de idade, não foi sequer mencionada.
Independentemente do gênero, todos temos a mesma capacidade intelectual, mas cada indivíduo tem fórmas diferentes de entender a natureza. Essa diversidade ajuda a Ciência a conseguir mais e melhores respostas para seus questionamentos.


ATIVIDADES
REGISTRE EM SEU CADERNO
- Cite as mulheres cientistas que você conhece. Cite também os homens cientistas. Há diferença na quantidade de nomes mencionados entre os gêneros?
- A importância da pesquisa de Rosalind Fránklin não foi devidamente reconhecida em sua vida. Porém, como fórma de reparação histórica em reconhecimento à importância de seu trabalho para o estudo da vida, a Agência Espacial Europeia (ê ésse á) batizou com seu nome o robô da Missão ExoMars, que buscará por registros de vida antiga em Marte. Em grupos, pesquisem outro exemplo de reparação histórica na Ciência, ou no ensino de Ciência, para uma mulher, para um grupo de mulheres ou para as mulheres em geral.
• Depois, compartilhem as descobertas com o restante da turma e, sob a orientação do professor, façam um debate sôbre a importância das reparações históricas para a Ciência e para a sociedade.
Respostas e comentários
Orientações didáticas
• A seção Pensar Ciência busca estimular a troca de ideias sôbre a participação feminina na Ciência. É importante ouvir a opinião dos estudantes e incentivar a argumentação e a reflexão embasadas em dados e no respeito a todas as pessoas. Essa abordagem permite mobilizar as competências gerais 7 e 9 da Educação Básica e as competências específicas 4 e 5 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê. Ao promover a reflexão sôbre a participação das mulheres nos diversos setores da sociedade, trabalha-se o tê cê tê – Educação em Direitos Humanos.
• A fim de contribuir com o processo de geração de inferências, sugerimos trabalhar a atividade 1 dessa seção antes da leitura do texto. Essa é uma ação preliminar que pode conduzir os estudantes a desenvolverem uma leitura mais aprofundada e uma melhor compreensão do texto a ser lido.
Respostas – Pensar Ciência
1. É provável que os estudantes conheçam ou já tenham ouvido falar de mais nomes de cientistas homens do que de cientistas mulheres. Caso isso tenha acontecido, pergunte a eles por que acham que houve essa diferença e se algo deveria ser feito para mudar esse cenário.
2. Antes que os estudantes iniciem esta atividade, peça-lhes para pesquisar o significado de “reparação histórica”. Depois, durante a mediação do debate, oriente-os a ouvir os colegas com atenção e a interagir com os demais de fórma respeitosa.
Sugestão de recurso complementar
Artigo
MARASCIULO, M. “Mulheres eram consideradas sem cérebro”, diz física que revolucionou astronomia. Galileu, 15 julho 2022.
O texto conta brevemente a história de (1943-), que descobriu os pulsares em 1967. Alguns anos depois, dois homens foram premiados com o Nobel de Física por essa descoberta, e o nome da pesquisadora nem sequer foi mencionado. Como reparação histórica, em 2018 ela recebeu o prêmio Breakthrough de Física, considerado um Nobel alternativo.
Disponível em: https://oeds.link/YHLoye. Acesso em: 13 agosto 2022.

Atitudes para a vida
REGISTRE EM SEU CADERNO
Descarte de medicamentos no lixo comum pode contaminar o meio ambiente
O hábito de manter em casa uma pequena farmácia nos momentos de necessidade pode ser útil, mas também causa problemas. Quando o prazo de validade dos medicamentos chega ao fim, reticências o descarte do fármaco no lixo comum leva à contaminação do meio ambiente.
reticências
Se o medicamento está vencido, o correto é descartá-lo. Porém, isso deve ser feito de fórma especial, para que não haja contaminação do solo nem da água. De acôrdo com a doutoranda em Biologia, Gabrielle Rabelo Quadra, o risco é real.
“Esse material pode ir para um aterro sanitário, formar o chorume e chegar ao subterrâneo, contaminando o lençol freático. Se for para o esgôto não tratado, o fármaco chega direto ao meio ambiente. Caso o esgôto seja tratado, as estações não são feitas para remover fármacos completamente, e fica um resíduo. Isso pode ser prejudicial a animais e a seres humanos.”
reticências
Fonte: Descarte de medicamentos no lixo comum pode contaminar o meio ambiente. ú éfe jota éfe Notícias, 15 março2017. Disponível em: https://oeds.link/SEoeO6. Acesso em: 7 agosto 2022.

Respostas e comentários
Orientações didáticas
• A seção Atitudes para a vida traz a discussão a respeito do descarte correto de resíduos, especificamente de medicamentos fóra da validade. Essa é uma oportunidade de os estudantes perceberem que podem colaborar com a conservação do ambiente estando atentos às atitudes que tomam em seu cotidiano, como o descarte adequado de medicamentos. Assim, ao avaliar os impactos ambientais do descarte incorreto de medicamentos e buscar agir para promover mudanças individuais e coletivas, recorrendo aos conhecimentos de Ciências da Natureza, os estudantes terão subsídios para desenvolver as competências gerais 2, 4, 9 e 10 da Educação Básica e as competências específicas 3 e 8 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê.
• É provável que os estudantes tenham conhecimentos sôbre a reciclagem e o descarte adequado de materiais como o lixo eletrônico. Retome esses conhecimentos para introduzir a discussão sôbre o descarte correto de medicamentos, possibilitando assim a geração de inferências enquanto leem o texto desta seção.
• Peça aos estudantes que pesquisem como deve ser feito o descarte de medicamentos vencidos em seu município. Devido à falta de uma regulamentação federal para o assunto, existem municípios que, por fôrça de lei, determinam que qualquer farmácia receba esse tipo de material e encaminhe para o descarte correto. Em outros locais, as unidades de saúde recebem o material. Existem ainda iniciativas de empresas, como redes de farmácias, que fazem o recolhimento e providenciam o descarte correto.
• Explique à turma que, no momento em que a validade do remédio expira, não existe mais garantia da qualidade do produto. Além de não produzir o efeito esperado do medicamento, seu uso pode até mesmo causar efeitos indesejáveis e inesperados no organismo.
Sugestão de recurso complementar
Artigo
ANDRADE, E. D. Prazo de validade dos medicamentos. Implant News, 20 setembro 2020.
O texto traz informações importantes sôbre o prazo de validade dos medicamentos.
Disponível em: https://oeds.link/ubioWa
Acesso em: 12 agosto 2022.
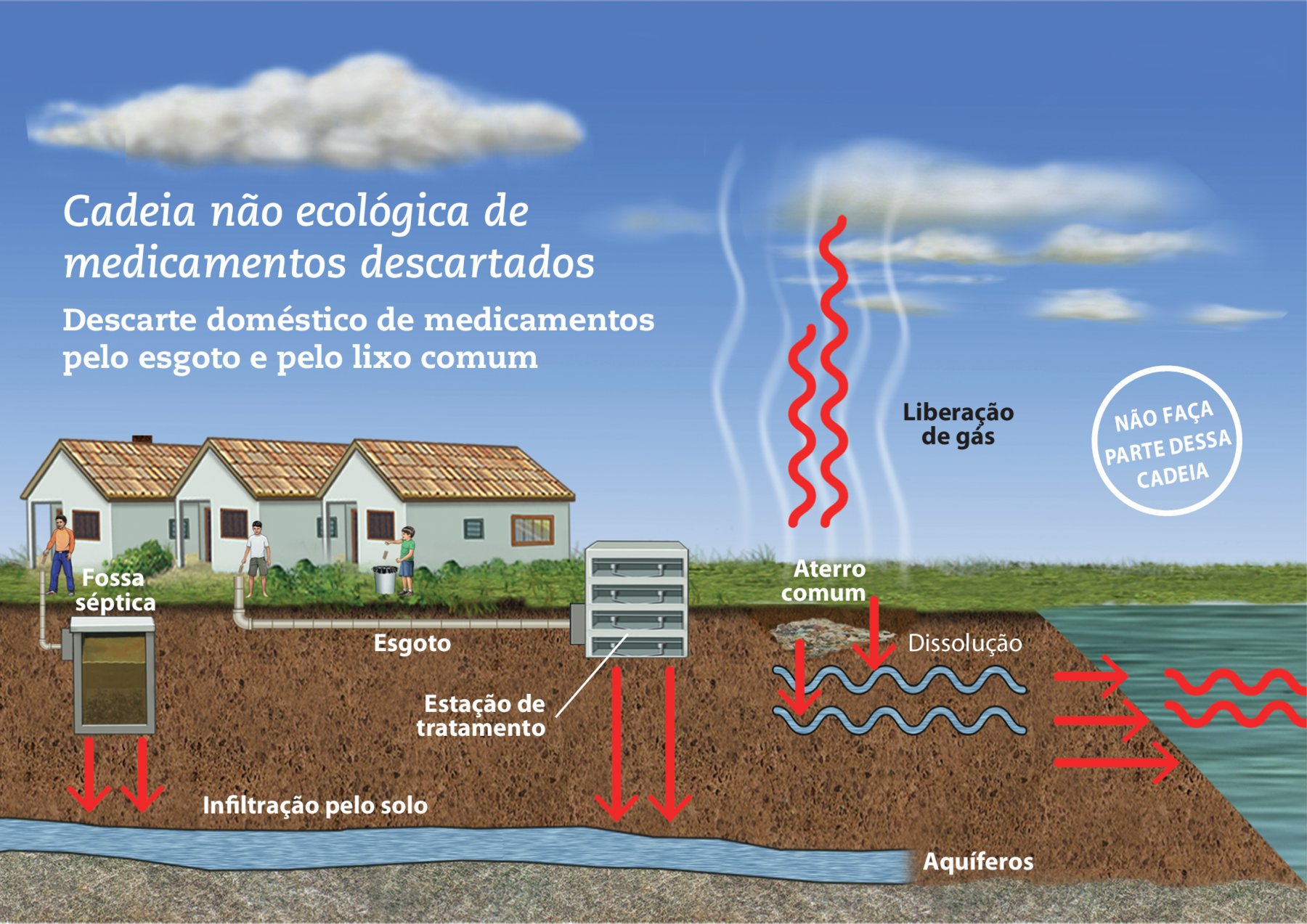
Fonte: BRASIL HEALTH SERVICE. O problema ambiental: cadeia não ecológica de medicamentos descartados. Programa descarte consciente. Disponível em: https://oeds.link/TrzCzV. Acesso em: 7 agosto 2022.
TROCAR IDEIAS sôbre O TEMA
Em grupo, discutam as seguintes questões:
- A responsabilidade pelo descarte correto de medicamentos deve ser somente dos fabricantes dêsses produtos?
- Como podemos contribuir para evitar a contaminação do ambiente pelos medicamentos?
COMPARTILHAR
- Forme um grupo com mais dois colegas. Cada integrante do grupo deverá entrevistar os familiares responsáveis e anotar as respostas dadas às perguntas indicadas a seguir.
- De que maneira os medicamentos vencidos ou que não foram usados são descartados?
- Você acha que os medicamentos descartados diretamente no lixo ou na rede de esgôto podem contaminar a água de rios e lagos?
- De que maneira os medicamentos vencidos ou que não foram usados são descartados?
Compartilhem com os demais colegas as respostas obtidas nas entrevistas. Em seguida, discutam suas opiniões diante das respostas coletadas. Proponham medidas que poderiam ajudar a minimizar o problema do descarte incorreto de medicamentos. Elaborem um documento contendo os prejuízos da contaminação de rios e lagos, a importância de conservar a natureza em prol da nossa saúde e as propostas da turma. Esse documento poderá ser divulgado à comunidade em formato impresso ou digital após aprovação do professor.

COMO EU ME SAÍ?
- Contribuí com a discussão coletiva?
- Usei conhecimentos que já tinha para obter soluções aos questionamentos propostos?
- Se fosse explicar por que aplicar conhecimentos prévios a novas situações é importante, eu diria...
Respostas e comentários
Orientações didáticas
• Auxilie os estudantes na análise da imagem “Cadeia não ecológica de medicamentos descartados”, a fim de que eles compreendam as fórmas pelas quais os medicamentos, quando descartados de maneira incorreta, prejudicam o ambiente.
• A atividade 3 permite aos estudantes que levantem dados a respeito do tema por meio de uma entrevista e que, então, analisem esses dados e discutam suas opiniões, para depois propor uma solução prática para um problema da comunidade. As atividades dessa seção perpassam pelo tê cê tê – Educação Ambiental. Além disso, favorecem o desenvolvimento da competência geral 9 da Educação Básica, da competência específica 8 de Ciências da Natureza para o Ensino Fundamental e da habilidade ê éfe zero nove cê ih um três, previstas pela Bê êne cê cê.
Respostas – Atitudes para a vida
1. O fabricante deve se responsabilizar pelo recolhimento e destruição ou pela reciclagem do material vencido. No entanto, cabe ao consumidor levar os medicamentos vencidos aos postos de coleta.
2. Não descartar os medicamentos de maneira incorreta e instruir aqueles com quem convivemos a agir da mesma fórma.
3. Por meio da entrevista e do compartilhamento das respostas obtidas, a atividade possibilita aos estudantes o levantamento e a análise de dados. Espera-se que os estudantes compreendam a importância de participar ativamente de ações para a conservação do ambiente, tanto com atitudes individuais, como o descarte correto de medicamentos como com atitudes coletivas, comunicando à outras pessoas a importância dessas ações e propondo medidas para minimizar os problemas ambientais da comunidade.

Compreender um texto
Aumento do nível do mar e aquecimento global: como evitar o pior cenário?
O Painel Intergovernamental sôbre Mudanças Climáticas (í pê cê cê) é um órgão responsável por publicar relatórios os quais compilam os últimos estudos sôbre as mudanças climáticas que afetam o planeta, em todas as esferas e cenários.
De acôrdo com as projeções da primeira parte do relatório, publicada em 2021, a temperatura média na América do Sul, por exemplo, deve subir mais rápido que a média do planeta.
Os cientistas acreditam que um aumento de 1,5 graus Célsius acima dos níveis pré-industriais será alcançado até 2040, podendo ultrapassar os 2 graus Célsius até o fim do século 21. Considerando que o tratado firmado no acôrdo de Paris prevê a manutenção da temperatura média global neste século abaixo de 2 graus Célsius – sendo 1,5 graus Célsius o limite ideal –, é preciso urgentemente que medidas mais drásticas sejam adotadas para reduzir a emissão de gases do efeito estufa. Apesar das evidências científicas e dos eventos climáticos extremos terem acontecido com cada vez mais frequência (ondas de calor, incêndios, chuvas intensas e sêcas prolongadas), as iniciativas dos governos e das grandes empresas parecem não estar à altura da urgência da ação, e assim as emissões de gases-estufa continuam a crescer.
Variação da temperatura em graus Célsius nas diferentes regiões do planeta entre 1971 e 2021
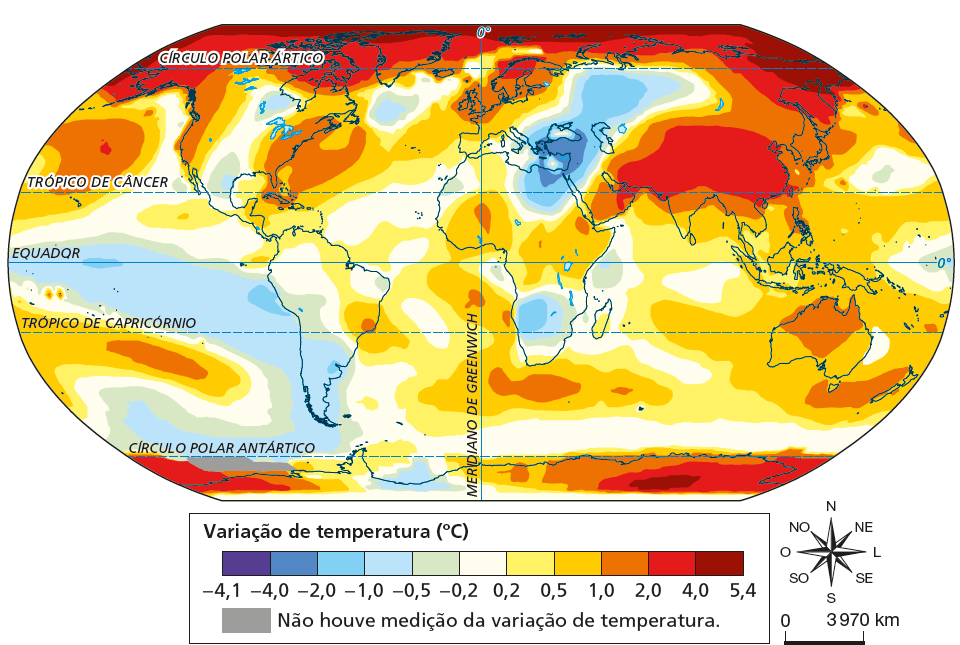
Fonte: Náza. GISS Surface Temperature AnalysesGlobal Maps from GHCN (). Goddard Institute for Space Studies Disponível em: https://oeds.link/7sHfzX. Acesso em: 7 agosto 2022.
Respostas e comentários
Orientações didáticas
• Verifique o entendimento do que foi lido por meio da inferenciação, ou seja, os novos elementos e conceitos gerados a partir das fontes de informações (conhecimentos prévios e o conteúdo do texto). Avalie as respostas dos estudantes individualmente e, depois, trabalhe novamente com toda a turma aquelas em que notou mais dificuldades. Faça com eles a interpretação do conteúdo dessas atividades, ressaltando e discutindo os erros mais comuns.
• Antes de orientar os estudantes a fazer uma leitura silenciosa do texto, verifique os conhecimentos da turma sôbre o efeito estufa e o acôrdo de Paris. Explique que existem encontros e conferências internacionais com o objetivo de que os países façam acordos para resolver problemas ambientais de âmbito mundial, como o aquecimento global. A necessidade dêsses eventos se deve às negociações e ao convencimento que deve ser feito para que os países não assumam posturas individualistas e concordem em rever aspectos políticos e econômicos para o bem comum. As atividades dessa seção favorecem o desenvolvimento das competências gerais 6 e 7 da Educação Básica e das competências específicas 3 e 4 de Ciências da Natureza para o Ensino Fundamental, previstas pela Bê êne cê cê.
• Faça com os estudantes a leitura do mapa “Variação da temperatura em graus Célsius nas diferentes regiões do planeta entre 1971 e 2021”. Repare que, apesar de a temperatura média do planeta ter aumentado nesse período, pode-se verificar no mapa que em algumas regiões a temperatura diminuiu. No entanto, os maiores aumentos foram registrados, entre outras regiões, no Ártico, o que provocou o derretimento de geleiras.
• De fórma interdisciplinar com o componente curricular Língua Portuguesa, trabalhe com o gênero textual reportagem. A análise dos mapas pode ser trabalhada de fórma interdisciplinar com os componentes curriculares Geografia e História.
Outro fenômeno analisado pelos cientistas, devido ao aquecimento, é o derretimento de geleiras, acarretando o aumento do nível do mar.
Segundo o relatório, as mudanças projetadas em um cenário positivo estimam um aumento do nível do mar de 43 centímetros até 2100. Já em um cenário mais adverso a elevação do nível do mar chegaria a 84 centímetros.
Fontes: , Éme outrosSea Level Rise and Implications for Low-Lying Islands, Coasts and Communities. In: IPCC Special Report on the Ocean and Cryosphere in a Changing Climate, 2019. Disponível em: https://oeds.link/rWCpE5 ABRAM, Framing and Context of the Report.In: IPCC Special Report on the Ocean and Cryosphere in a Changing Climate, 2019. Disponível em: https://oeds.link/A7TnZ9. Acessos em: 7 agosto2022.
Mudanças pretéritas e futuras no oceano
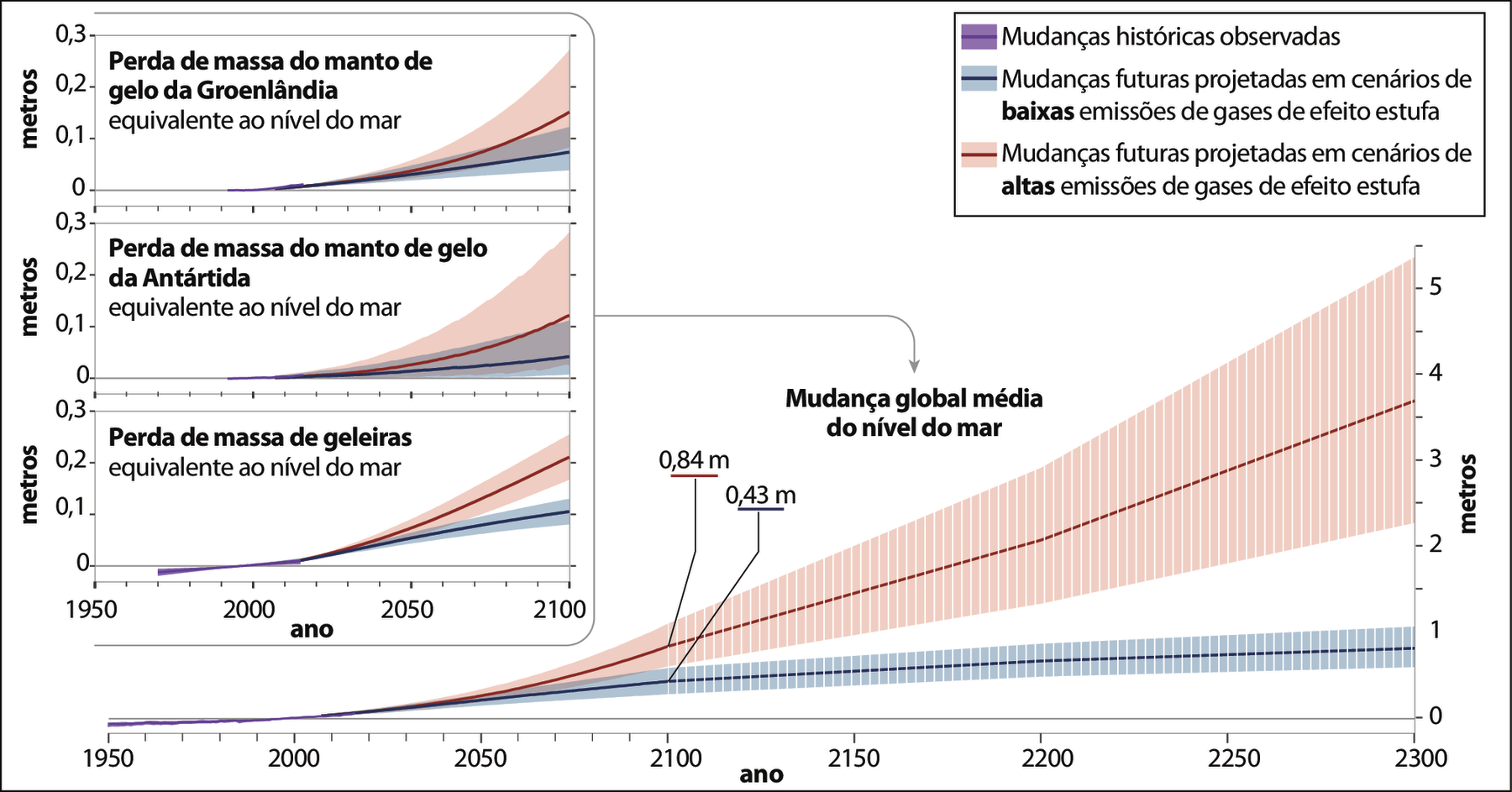
Fonte: BRASIL. O oceano e a criosfera em um clima em mudança. Um Relatório Especial do Painel Intergovernamental sôbre Mudança do Clima. [Tradução realizada pelo govêrno do Brasil], página 12, 2019. Disponível em: https://oeds.link/boPFTr//www.ipcc.ch/site/assets/uploads/sites/3/2020/11/SROCC_SPM_Portuguese.pdf. Acesso em: 7 março 2022.

ATIVIDADES
REGISTRE EM SEU CADERNO
OBTER INFORMAÇÕES
- Qual foi a maior variação de temperatura entre 1971 e 2021 medida no território brasileiro?
- Quais contribuições cada um de nós pode dar para a redução da emissão dos gases de efeito estufa?
INTERPRETAR
3. Analisando o gráfico, o que deve acontecer com o nível médio dos oceanos até 2100?
REFLETIR
- Pesquise se há consenso sôbre as causas do aquecimento global no meio científico e em outros setores da sociedade. Caso não haja consenso em algum dêsses setores, quais são os argumentos para explicar os dados apresentados pelo texto? Você considera esses argumentos válidos?
- Em sua opinião, por que alguns países se recusam a assumir compromissos para a redução de seus poluentes?
Respostas e comentários
Orientações didáticas
• O gráfico, resultante de registros históricos e das projeções realizadas pelo í pê cê cê, mostra o aumento do nível do mar decorrente da perda de massa de gêlo da Groenlândia e da Antártida. É importante que os estudantes compreendam que no gráfico há duas projeções, para cenários de altas e para cenários de baixas emissões de gases de efeito estufa.
Respostas – Compreender um texto
1. Entre 1 grau Célsius e 2 graus Célsius.
2. Diminuir o consumo de energia em nossa moradia, andar a pé ou de bicicleta, reduzir o consumo, reutilizar materiais e reciclar são algumas atitudes que podem contribuir para a redução da emissão dêsses gases.
3. O nível dos oceanos deverá aumentar até o final deste século em decorrência de fatores como o derretimento das geleiras.
4. Atualmente há consenso na comunidade científica de que o aquecimento global deve-se a causas antrópicas, resultado das emissões de gases de efeito estufa pelos seres humanos. Entretanto, alguns setores da sociedade contestam essa visão ou, até mesmo, a própria ocorrência do aquecimento global. Estimule os estudantes a refletir sôbre a confiabilidade das fontes de informação que eles encontraram durante suas pesquisas e oriente-os sôbre os critérios para considerar uma fonte confiável ou não. Com relação aos argumentos encontrados, caso apontem causas não antrópicas do aquecimento global ou sua inexistência, é provável que se trate de argumentos falaciosos por basearem-se em dados desatualizados, incompletos ou incorretos. Estimule e oriente os estudantes a conferir esses argumentos utilizando dados científicos atualizados.
5. A base da economia de alguns países está estabelecida em processos produtivos altamente poluentes, e um dos argumentos utilizados por líderes dessas nações é o de que a redução de poluentes resultaria na diminuição da produtividade e do desenvolvimento econômico.
Sugestões de recursos complementares
Artigo
, A. L.; MASSONI, N. T. O consenso científico sôbre aquecimento global antropogênico: considerações históricas e epistemológicas e reflexões para o ensino dessa temática. Revista brasileira de pesquisa em educação em ciências, Porto Alegre. volume18, número2, página 455-491, agosto2018.
O artigo discute a abordagem do aquecimento global no ensino de Ciências e a cautela necessária ao se tratar esse tema como controverso no meio científico.
Disponível em: https://oeds.link/F4AlgO
Site
. í pê cê cêa Sea Level Projection Tool.Sea level change: observations from space.
A página (em inglês) disponibiliza uma ferramenta de visualização que mostra os dados sôbre o aumento futuro do nível do mar em qualquer lugar do oceano ou da costa.
Disponível em: https://oeds.link/KoZG62
Acessos em: 12 agosto 2022.
Glossário
- Macroscópico
- : tudo o que pode ser observado a ôlho nu.
- Voltar para o texto